
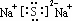 .
.分析 (1)短周期中含有金属元素和非金属元素的周期是2、3周期,氢氧化铝是两性氢氧化物;
(2)硫化钠是钠离子和硫离子之间通过离子键形成的离子化合物;
(3)氯气具有氧化性,能将二氧化硫氧化为硫酸;
(4)微粒半径大小的比较方法:电子层越多半径越大,核外电子数一样时,质子数越多半径越小,反之越大;
(5)同周期元素,从左到右,失电子能力逐渐减弱,金属性逐渐减弱;
解答 解:(1)同一短周期含有金属元素和非金属元素的周期是2、3周期,A、B各自的最高价氧化物对应的水化物可以反应生成盐和水,所以A是金属钠,B是金属铝,氢氧化钠和氢氧化铝的反应为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)Na与C可形成化合物Na2C,所以C显-2价,在该周期中,所以C是S碳元素,硫化钠是离子化合物,电子式为: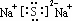 ,
,
故答案为: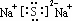 ;
;
(3)C是S碳元素,则D是Cl,S的低价氧化物是二氧化硫,通入Cl2的水溶液中,发生氧化还原反应,其反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl,
故答案为:SO2+Cl2+2H2O=H2SO4+2HCl;
(4)硫离子和氯离子电子层数多,钠离子和铝离子电子层数少,电子层越多半径越大,核外电子数一样时,质子数越多半径越小,反之越大,即S2->Cl->Na+>Al3+,
故答案为:S2->Cl->Na+>Al3+;
(5)同周期元素,从左到右,失电子能力逐渐减弱,金属性逐渐减弱,所以金属性最强的是Na,非金属性最强的是Cl,
故答案为:Na;Cl;
点评 本题是一道考查元素周期律的综合知识题目,可以根据所学知识进行回答,难度较大,综合性较强.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:解答题
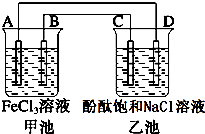 如图所示,甲池中电池反应式为2Fe3++Cu═2Fe2++Cu2+,反应过程中A电极质量逐渐减小,C、D为石墨电极,乙池中为200mL滴加酚酞的饱和NaCl溶液.回答下列问题:
如图所示,甲池中电池反应式为2Fe3++Cu═2Fe2++Cu2+,反应过程中A电极质量逐渐减小,C、D为石墨电极,乙池中为200mL滴加酚酞的饱和NaCl溶液.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
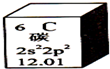 元素周期表是学习化学的重要工具.下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具.下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )| A. | 该元素的三种核素质子数均为6 | B. | 该元素原子最外层有4个电子 | ||
| C. | 该元素的相对原子质量为12.01 | D. | 该元素的原子核外有三个电子层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
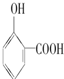
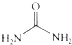 的熔、沸点比醋酸
的熔、沸点比醋酸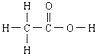 的高.
的高.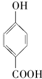 >
>
| A. | ①②③④⑤⑥ | B. | ①②③④⑤ | C. | ①②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要鉴别己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 | |
| B. | 配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 | |
| C. | 制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 | |
| D. | 除去溴苯中少量的溴,可以加水后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
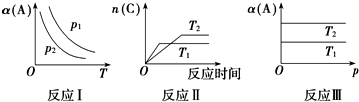
| A. | 在图象反应Ⅰ中,说明正反应为吸热反应 | |
| B. | 在图象反应Ⅰ中,若p1>p2,则此反应的△S>0 | |
| C. | 在图象反应Ⅱ中,说明该正反应为吸热反应 | |
| D. | 在图象反应Ⅲ中,若T1>T2,则该反应能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
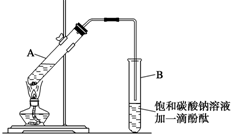 已知下表所示数据:
已知下表所示数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | 338.0 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a+3b | B. | $\frac{a}{2}$+3b | C. | $\frac{a}{2}$+3b+$\frac{7w}{2}$ | D. | $\frac{a}{2}$+3b-$\frac{7w}{2}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二者都能使溴的四氯化碳溶液褪色 | B. | 二者互为同系物 | ||
| C. | 二者实验式相同 | D. | 聚乙烯是乙烯的缩聚产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com