
| A. | 氢氧化物呈两性 | B. | 单质与水反应放出氢气 | ||
| C. | 在化合物中呈+2价 | D. | 单质的还原性比镁强 |
分析 镭是元素周期表中第七周期的ⅡA族元素,最外层有2个电子,性质活泼,易与水反应,利用同主族元素性质的递变规律以及同主族元素性质具有相似性分析,可以结合熟悉的金属镁、钙和钡的性质来回答.
解答 解:A、同主族从上到下,金属性逐渐增强,最高价氧化物对应水化物的碱性增强,氢氧化钡是强碱,所以镭的氢氧化物是强碱,故A错误;
B.同主族元素从上到下金属性逐渐增强,镭的金属性较强,单质性质活泼,与水反应放出氢气,故B正确;
C.镭最外层有2个电子,在化合物中呈+2价,故C正确;
D.同周期从上往下金属性增强,所以单质的还原性比镁强,故D正确;
故选A.
点评 本题考查同主族元素的性质的递变规律,从同主族元素金属性对应单质、化合物的性质的相似性和递变性的角度解答该题,难度不大,注意元素的金属性和非金属性的递变规律.


科目:高中化学 来源: 题型:选择题
| A | B | C | D |
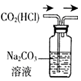 | 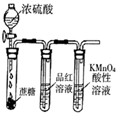 | 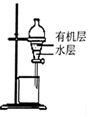 | 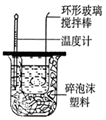 |
| 除去CO2中含有的少量HCl气体 | 说明浓H2SO4具有脱水性,强氧化性,SO2具有漂白性、还原性 | 将有机层从分液漏斗下口放出 | 用于中和反应反应热的测定 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①②④ | C. | ②③⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥⑦ | B. | ③④⑥⑦ | C. | ①②④⑥⑦ | D. | ①②⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>③>②>① | B. | ④>③>①>② | C. | ②>③>④>① | D. | ②>④>③>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
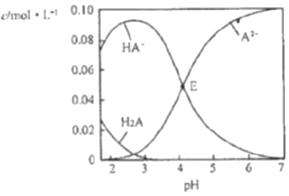
| A. | pH=2的溶液中:c(H2A)+c(A2-)>c(HA-) | |
| B. | E点溶液中:c(Na+)-c(HA-)<0.100mol•L-1 | |
| C. | c(Na+)=0.100mol•L-1的溶液中:c(H+)+c(H2A)=c(OH-)+c(A2-) | |
| D. | pH=7的溶液中:c(Na+)>2c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
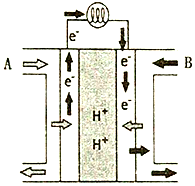 有X、Y、Z、W四种短周期元素,它们的核电荷数依次增大.只有Z是金属元素,X最外层只有一个电子,Y和W元素原子的最外层电子数相同,且Y元素原子L 层电子数是K层电子数的3倍,Z元素原子的最外层电子数是W元素原子最外层电子数的一半.请回答:
有X、Y、Z、W四种短周期元素,它们的核电荷数依次增大.只有Z是金属元素,X最外层只有一个电子,Y和W元素原子的最外层电子数相同,且Y元素原子L 层电子数是K层电子数的3倍,Z元素原子的最外层电子数是W元素原子最外层电子数的一半.请回答: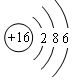 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2与H2在一定条件下合成NH3 | B. | NH3经催化氧化生成NO | ||
| C. | NO和O2反应生成NO2 | D. | 由NH3制碳铵和尿素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com