
����Ŀ��ijͬѧ����ͼ��ʾװ����ȡ�����ı���֤���÷�Ӧ��ȡ����Ӧ����ش�
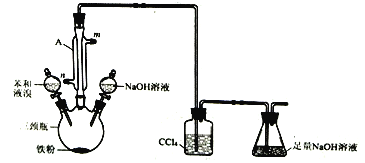
��1������A������Ϊ____________������ˮ�Ľ�ˮ��Ϊ_________��(����m������n��)��
��2����ȡ�屽�Ļ�ѧ����ʽΪ___________________��
��3����ƿ������NaOH��Һ��������_________��
��4����ʵ�鰲ȫ�ĽǶȷ�������ʵ��װ�ô���һ�����Ե�ȱ����ָ��_________��
��5����Ӧ������������ƿ�еμ�����������Һ�������Ȼ����__________(����������)������屽(�Ժ���������)��
��6�����ʵ��֤����ȡ�屽�ķ�Ӧ��ȡ����Ӧ___________________��
���𰸡� ������ n ![]() �����廯�� ��ƿ�ڵij����ܵĹܿڲ�Ӧ������Һ�� ��Һ©�� ȡ��Ӧ����ƿ�е���Һ�������Թ��У������еμ�AgNO3��Һ������������ɫ������˵��Ϊȡ����Ӧ
�����廯�� ��ƿ�ڵij����ܵĹܿڲ�Ӧ������Һ�� ��Һ©�� ȡ��Ӧ����ƿ�е���Һ�������Թ��У������еμ�AgNO3��Һ������������ɫ������˵��Ϊȡ����Ӧ
����������1������A������Ϊ�������ܣ�����ˮӦ��Ϊ�¿ڽ��Ͽڳ�����ˮ��Ϊn��
��2����ȡ�屽�Ļ�ѧ����ʽΪ��![]() ��
��
��3��ʵ���в�����HBrΪ�ж����壬��Ҫ����β����������ƿ������NaOH��Һ�������ǣ������廯�⡣
��4���廯���������������Ʒ�Ӧ�����������ʸ�ʵ��װ���е�ȱ���ǣ���ƿ�ڵij����ܵĹܿڲ�Ӧ������Һ�С�
��5����Ӧ������������ƿ�еμ�����������Һ��������屽������ˮ��Ӧ���÷�Һ©�����з��룬�ʴ�Ϊ����Һ©����
��6��ȡ��Ӧ����ƿ�е���Һ�������Թ��У������еμ�AgNO3��Һ������������ɫ������˵��Ϊȡ����Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CaC2��ZnC2��Al4C3��Mg2C3��Li2C2��ͬ����������̼�����ͨ��CaC2��C2H2�ķ�Ӧ����˼�������еõ���Ҫ����ʾ���ж����з�Ӧ������ȷ����( )
A. Mg2C3ˮ�����ɱ�ȲB. Al4C3ˮ�����ɱ�Ȳ
C. ZnC2ˮ����������D. Li2C2ˮ��������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������KI��KCl������������ˮ�γ�1000mL��Һ��K+Ũ��Ϊ0.5mol��L-1����������ͨ��������Cl2����ȫ��Ӧ��������Һ���ɣ����յõ�����������ԭ����������������18.3g��
�Լ��㣺
��1��ԭ����������KI��������___
��2������������к���ʲô���ʣ�___�����ʵ����Ƕ��٣�___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϯ��������G�ڴ���ҩ��²��ϵȷ����й㷺Ӧ�á��ϳ�G��һ��·�����£�

��֪������Ϣ��
��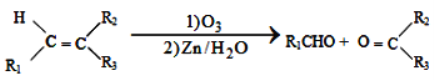
��1molB��������Ӧ������2molC����C���ܷ���������Ӧ��
��D���ڵ�ȡ��������������Է�������Ϊ106��
���˴Ź���������ʾF�����������ֻ�ѧ�������⡣
��
�ش��������⣺
��1����A����B�Ļ�ѧ����ʽΪ_______________________��
��2��D�Ļ�ѧ������______________________��
��3��G�Ľṹ��ʽΪ_______________________��
��4��F��ͬ���칹���к��б����Ļ���____�֣������������칹����
��5���ɱ��ͻ�����C�����²���ɺϳ�N-�����������
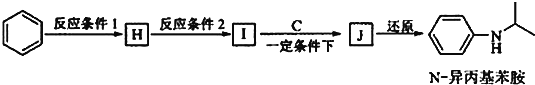
��Ӧ����2��ѡ�õ��Լ���_____________________�� I�Ľṹ��ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 18gD2O��18gH2O�к��е���������Ϊ10NA
B. 2L0.5mol/L��������Һ�к��е�H+��Ϊ2NA
C. 42g��ϩ�ͱ�ϩ�Ļ��������ȼ�����������ķ�����Ϊ4.5 NA
D. �ܱ�������2molNO��1molO2��ַ�Ӧ������ķ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. O2��O3 ����Ԫ�ص�ͬ�������壬���ʶ�����
B. 35Cl��37Cl-��Ϊͬλ��
C. �Ҷ���( ![]() ) ���ͣ�
) ���ͣ� ![]() ����Ϊͬϵ��
����Ϊͬϵ��
D. CH3CHO ��![]() ��Ϊͬ���칹��
��Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��V L Fe2(SO4)3��Һ�к���ag SO42-��ȡ����Һ0.5V L����ˮϡ����2V L����ϡ�ͺ���Һ��Fe3+�����ʵ���Ũ��Ϊ�� ��
A.![]() mol��L��1B.
mol��L��1B.![]() mol��L��1C.
mol��L��1C.![]() mol��L��1D.
mol��L��1D.![]() mol��L��1
mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л��ϳ��г��õ��ܼ���ijʵ��С����ʵ���������Ҵ���ˮ�Ʊ����ѣ�װ��ʾ��ͼ���гֺͼ���װ������ȥ�����й����ݺ�ʵ�鲽�����£�
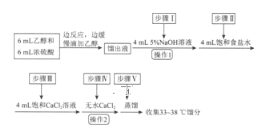

���� | ��Է������� | �ܶȣ���g��mL��1�� | �е㣯�� | ��ˮ�е��ܽ��� |
�Ҵ� | 46 | 0.816 | 78 | ���� |
���� | 74 | 0.713 | 34.6 | ���� |
��֪������ͬ�����£������ڱ���ʳ��ˮ�б���ˮ�и����ܡ�
���Ȼ��ƿ����Ҵ��γ������CaCl2��6C2H5OH��
��ش��������⣺
��1������B������Ϊ________��
��2�����Ҵ��Ʊ����ѵ��ܷ�ӦΪ2C2H5OH![]() CH3CH2OCH2CH3��H2O���˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH��H2SO4
CH3CH2OCH2CH3��H2O���˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH��H2SO4![]() CH3CH2OSO2OH��H2O����ڶ�����Ӧ�Ļ�ѧ����ʽΪ_____________��
CH3CH2OSO2OH��H2O����ڶ�����Ӧ�Ļ�ѧ����ʽΪ_____________��
��3������D��ʢ�б�ˮ����������Ϊ____________��
��4������1������Ϊ_______________��
��5����ʡ�Բ����ᵼ�µĺ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ka(CH3COOH)=1.75��10-5, Ka (HCN)=6.2��10-10������˵����ȷ����
A. 0.1mol/L CH3COONa��Һ��0.1mol/L KCN��Һ:c(Na+)-c(CH3COO-)> c(K+)-c(CN-)
B. 20mL0.1 mol/L CH3COONa��10mL 0.1 mol/L HCl��Һ��Ϻ�����������Һ:c(Na+)>c(CH3COOH)>c(CH3COO-)
C. 0.2 mol/LHCN��Һ��0.1 mol/L NaOH��Һ��������������Һ:c(Na+)>c(CN-)>c(OH-)>c(H+)
D. ��Ũ�Ⱦ�Ϊ0.1mol/L��CH3COOH��HCN�����Һ�еμ�0.1mol/LNaOH��Һ����ǡ���к�ʱ������Һ: c(CH3COOH)+c(HCN)+c(H+)=c(OH-)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com