
| A、标准状况下,22.4L己烷中共价键数目为19NA |
| B、2.4g镁在空气中充分燃烧所转移的电子总数为0.2NA |
| C、0.1 L1 mol/L的Na2CO3(aq)中CO32-与HCO3-的离子数之和为0.1NA.而1mol NaHSO4熔融产生离子总数3NA |
| D、0.5mol FeCl3滴入沸水可制备胶体粒子0.5 NA |


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
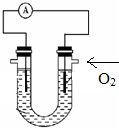 C、N、S的单质和化合物在工农业生产中有重要的应用.
C、N、S的单质和化合物在工农业生产中有重要的应用.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘化钾(碘):加热升华 |
| B、乙醇(水):加新制生石灰蒸馏 |
| C、二氧化碳(二氧化硫):通过氢氧化钠溶液 |
| D、乙酸乙酯(乙酸):加饱和碳酸钠溶液后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解过程中共消耗2amol水 | ||
| B、剩余溶液中有大量蓝色沉淀产生 | ||
C、剩余溶液中溶质的质量分数为
| ||
D、剩余溶液中溶质的质量分数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V(O2)=0.01mol/(L.s) |
| B、V(NO)=0.008mol/(L.s) |
| C、V(H2O)=0.0015mol/(L.s) |
| D、V(NH3)=0.002mol/(L.s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 |
| B、YX3的水溶液呈弱碱性,能使湿润的蓝色石蕊试纸变红 |
| C、原子半径:Z<Y<W,而简单离子半径:W<Y<Z |
| D、W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com