
一定温度下有:a.盐酸 b.硫酸 c.醋酸三种酸。
(1)当其物质的量浓度相同时,[H+]由大到小的顺序是______________。
(2)同体积、同物质的量浓度的三种酸,中和NaOH能力的顺序是____________。
(3)当其[H+]相同时,物质的量浓度由大到小的顺序为______________。
(4)当其[H+]相同、体积相同时,分别加入足量锌,相同状况下产生气体的体积由大到小的顺序为_________________________________________________________________。
(5)当[H+]相同、体积相同时,同时加入锌,若产生相同体积的H2(相同状况),则开始时的反应速率________,反应所需时间__________。
(6)将[H+]相同的三种酸均稀释10倍后,[H+]由大到小的顺序是______________。
科目:高中化学 来源: 题型:
下列各组离子能在指定溶液中大量共存的是( )
①无色溶液中:Al3+,Cl-,Na+,HCO3-,SO42-
②使pH=11的溶液中:Na+,AlO2-,NO3-,S2-,SO32-
③加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
④使pH试纸呈红色的溶液中:Fe3+,MnO4-,Na+,SO42-
⑤酸性溶液中:Fe2+,Al3+,NO3-,I-
A.①②④ B.①⑤ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
由乙醇制乙二酸乙二酯最简单的正确流程途径顺序是( )
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应 ⑦水解反应
A.①②③⑤⑦ B.⑤②⑦③⑥
C.⑤②①③④ D.①②⑤③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组探究FeSO4的化学性质和用途。回答下列问题:
(一) 探究FeSO4溶液的酸碱性:
38.取少量FeSO4固体,利用石蕊试液测试FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和 。
A.玻璃棒 B.试管 C.天平 D.量筒
(二)利用下图装置探究FeSO4的稳定性
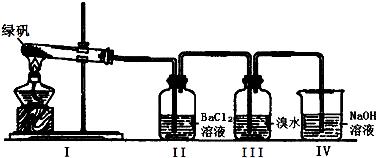
39. II中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是 。
A.Fe2O3、SO3、H2O B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
40. III中溴水是用来检验是否有SO2气体生成,若有SO2生成,溴水将褪色。实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是 。
41. NaOH的作用是吸收SO2气体,请写出最大量吸收SO2气体的反应化学方程式: 。
(三)探究FeSO4中Fe2+还原性:
42. 证明FeSO4有较强的还原性,完成下表。
| 实验步骤 | 实验预期现象及结论 |
| 步骤一:取少量的FeSO4固体于试管中,加入一定量水溶解。 |
|
| 步骤二: |
|
(四)硫酸亚铁用途探究
43. 缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子一定能大量共存的是( )
A.在含有大量[Al(OH)4]-的溶液中:NH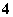 、Na+、Cl-、H+
、Na+、Cl-、H+
B.在强碱溶液中:Na+、K+、CO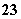 、NO
、NO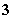
C.在pH=12的溶液中:NH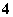 、Na+、SO
、Na+、SO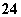 、Cl-
、Cl-
D.在[H+]=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO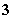
查看答案和解析>>
科目:高中化学 来源: 题型:
我国某大城市今年夏季多次降下酸雨.据环保部门测定,该城市整个夏季酸雨的pH平均为3.2.在这种环境中的铁制品极易被腐蚀.对此条件下铁的腐蚀的叙述不正确的是( )
|
| A. | 此腐蚀过程有化学腐蚀也有电化学腐蚀 |
|
| B. | 发生电化学腐蚀时的正极反应为 2H2O+O2+4e﹣═4OH﹣ |
|
| C. | 在化学腐蚀过程中有氢气产生 |
|
| D. | 发生电化学腐蚀时的负极反应为Fe﹣2e﹣═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中大量存在如下五种离子:NO3﹣、SO42﹣、Fe3+、H+、M,它们的物质的量之比依次为n(NO3﹣):n(SO42﹣):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M可能是( )
|
| A. | Al3+ | B. | Mg2+ | C. | CO32﹣ | D. | Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某溶液中由水电离的[H+]=1×10-13 mol·L-1,该溶液可能是( )
①三氧化硫水溶液 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行实验:
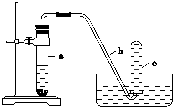
(1)在检查完装置的气密性后,向试管a中加入10 mL6 mol/L的稀HNO3和1 g Cu片,立即用带有导管的橡皮塞塞紧试管口,请写出在试管a中有可能发生的反应的化学方程式
_______________________________________________________________________________________________________________________________________________________________________________________________________________________。
(2)实验过程中常常反应开始时速率缓慢,随后逐渐加快,这是由于________________,当反应进行一段时间后速率又逐渐减慢,原因是________________________________________________________________________。
(3)欲较快地制得NO,可采取的措施是________。
A.加热 B.使用铜粉
C.稀释HNO3 D.改用浓HNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com