
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | NH4HCO3受热易分解,可用作氮肥 | |
| C. | 氢氧化铝具有弱碱性,可用作净水剂 | |
| D. | 常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 |
分析 A.二氧化硫具有漂白性;
B.NH4HCO3含N元素;
C.氢氧化铝胶体具有吸附性;
D.常温下Fe遇浓硝酸发生钝化,生成致密的氧化膜阻止反应的进一步发生.
解答 解:A.二氧化硫具有漂白性,可用于漂白纸浆,与其还原性无关,故A错误;
B.NH4HCO3含N元素,可用作氮肥,与其分解性无关,故B错误;
C.氢氧化铝胶体具有吸附性,则用作净水剂,与弱碱性无关,故C错误;
D.常温下Fe遇浓硝酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,则可用铁质容器贮运浓硝酸,故D正确;
故选D.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 用水洗涤2~3次后再使用 | |
| B. | 用滤纸擦干后才可使用 | |
| C. | 用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用 | |
| D. | 用盐酸洗涤后,经蒸馏水冲洗,方可使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 夜里的月色本身就很美 | |
| B. | 空气中的小水滴颗粒直径约为1nm-100nm | |
| C. | 光线是一种胶体 | |
| D. | 雾是一种胶体,能产生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56gFe与足量的盐酸反应,转移的电子数为2NA | |
| B. | 标准状况下,22.4L的水中含有的原子数为3NA | |
| C. | 物质的量浓度为2mol/L的BaCl2溶液中,含有Cl-个数为4NA | |
| D. | 22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
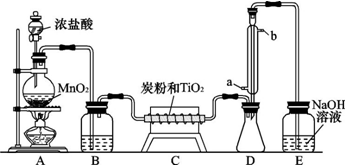
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
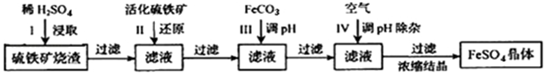
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
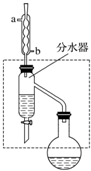 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.0 |
| 密度/g•cm-3 | 1.1 | 0.80 | 0.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
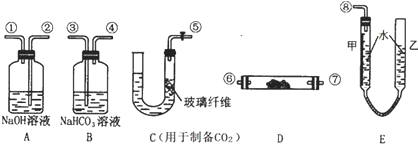
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com