
| X | Y | Z | |
| A | NaHCO3溶液 | Na2CO3 | Ba(OH)2溶液 |
| B | Fe2O3 | Al2O3 | NaOH溶液 |
| C | FeCl3溶液 | CuCl2 | Fe |
| D | Na2SO4溶液 | Na2CO3 | 盐酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.反应生成NaCl,引入新杂质;
B.Al2O3为两性氧化物,可与氢氧化钠反应;
C.FeCl3和CuCl2都可与Fe反应;
D.加入盐酸引入新杂质.
解答 解:A.加入BaCl2溶液,可除去Na2CO3,但反应生成NaCl,引入新杂质,应通入二氧化碳气体除杂,故A错误;
B.Al2O3为两性氧化物,可与氢氧化钠反应,可用于除杂,故B正确;
C.FeCl3和CuCl2都可与Fe反应,最终生成FeCl2,应再滴加氯水,故C错误;
D.加入盐酸引入新杂质,应加硫酸,故D错误.
故选B.
点评 本题考查物质的分离、提纯,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意除杂时不能引入新的杂质,更不能影响被提纯的物质的性质,难度不大.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:解答题

 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定某化学反应反应速率的主要因素是催化剂 | |
| B. | 青霉素、橡胶、阿斯匹林全部由化学合成制得 | |
| C. | 铝有还原性,在反应中放出大量热能用来冶炼难熔金属Mn等 | |
| D. | 陶瓷品、酒精、乙烯塑料等的使用不会对环境造成污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸发、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol/LNaCl溶液 | B. | 1L3mol/LNa2SO4溶液 | ||
| C. | 0.4mol/LNaOH溶液 | D. | 2L0.15mol/LNa3PO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
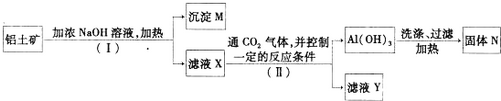
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 含1molHCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为2NA | |
| C. | 常温常压下,32gO2和32gO3所含氧原子数都是2NA | |
| D. | 1mol/L的Na2SO4溶液中含2NA个Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LNO与11.2LO2混合,混合气体所含分子数为NA | |
| B. | 1molAl3+含有的核外电子数为10NA | |
| C. | 常温常压下,1mol氮气含有的原子总数为NA | |
| D. | 1L1mol/LFeCl3溶液全部制成胶体,其中含胶粒的数目小于NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com