
| ѡ�� | ʵ����������� | ���� |
| A | ��Fe��NO3��2����ϡH2SO4�μ�KSCN��Һ�� ��Һ��ɺ�ɫ | Fe��NO3��2��һ����Fe3+ |
| B | ��ú����ȡ��һС���ƣ�����ֽ���������ú�ͣ� ������ˮ�Ҵ��У��������� | Na���û����������е��� |
| C | ��ij����ͨ��Ʒ����Һ����Һ��ɫ | ����һ����SO2 |
| D | ��NaAlO2��Һ�е���NaHCO3��Һ��������ɫ���� | AlO2-���H+��������CO32-ǿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��Fe��NO3��2����ϡH2SO4����������ԭ��Ӧ���������ӣ�
B�������Ҵ���Ӧ�����Ҵ��ƺ�������
C������Ư���Ե����ʿ�ʹƷ����ɫ��
D����NaAlO2��Һ�е���NaHCO3��Һ����������������̼���ƣ�
��� �⣺A��Fe��NO3��2����ϡH2SO4����������ԭ��Ӧ���������ӣ�Ӧ����ˮ�����Ƿ������ӣ���A����
B�������Ҵ���Ӧ�����Ҵ��ƺ������������������۾���������B��ȷ��
C������Ư���Ե����ʿ�ʹƷ����ɫ��������Ϊ�������������ȣ���C����
D����NaAlO2��Һ�е���NaHCO3��Һ����������������̼���ƣ���AlO2-���H+��������CO32-ǿ����D��ȷ��
��ѡBD��
���� ���⿼�黯ѧʵ�鷽�������ۣ�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ������ʵ�����Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ��������Է�������Ŀ�ѶȲ���


 �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д� С����ȫ�ܼ��ϵ�д�
С����ȫ�ܼ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BaSO4��BaCO3�ܽ��С������BaCO3������ת��ΪBaSO4 | |
| B�� | BaCO3��BaSO4��������ˮ�����Զ������������Լ� | |
| C�� | ���¶��£�BaCO3��Ҫ��Na2SO4��Һ��ת��ΪBaSO4����Na2SO4Ũ������Ϊ2.2��10-6 mol•L | |
| D�� | �κ��¶��£���Na2CO3��Һ�м���BaCl2��Na2SO4�������ֳ�������ʱ��c��SO42-��/c��CO32-��=4.4��10-3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Ӧ�Ͻ��̻� | |
| B�� | NH3й¶ʱ���������ˮ�� | |
| C�� | ��Cl2��β���ü���Һ���������ŷ� | |
| D�� | ������ʧ��ʱӦ�����ô�����ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
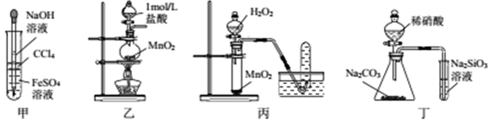
| A�� | �ü���ʾװ����ȡ���۲�Fe��OH��2 | |
| B�� | ������ʾװ����ȡ����Cl2 | |
| C�� | �ñ���ʾװ����ȡO2 | |
| D�� | �ö���ʾװ�ñȽ�N��C��Si�ķǽ�����ǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��FeCl3��Һ��ʴͭ�壺Fe3++Cu�TFe2++Cu2+ | |
| B�� | ��ˮ��ͨ�����SO2��SO2+2NH3•H2O�T2NH4++SO32-+H2O | |
| C�� | ��MnO2��Ũ���ᷴӦ��Cl2��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2Cl-+Cl2��+2H2O | |
| D�� | ��ǿ������Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+2Fe��OH��3+4OH-�T2FeO43-+3Cl-+5H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
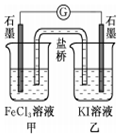
| A�� | ��������������ʴʱ������ʴ�����ʺ�����Ũ���� | |
| B�� | ��״���£�2.24LCCl4�����й��ۼ�����ĿΪ0.4��6.02��1023 | |
| C�� | �����ʺϵ�����������Ӧ2Fe3++2I-�T2Fe2++I2��Ƴ���ͼ��ʾ��ԭ��أ�������֭����Ϊ����ڼ�������FeCl2���壬������ʯī�缫Ϊ���� | |
| D�� | ��ʢ��2mL����H2S��Һ����֧�Թ��зֱ�μ�1��Ũ�Ⱦ�Ϊ0.1mol/L��ZnSO4��Һ��CuSO4��Һ����CuS���ɶ���ZnS���ɣ���Ksp��CuS����Ksp��ZnS�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ҽ�þƾ���ʹ�����ʱ��ԣ�����������ɱ�� | |
| B�� | SiO2�кܺõ��۹��ʣ������������뵼����� | |
| C�� | ˮ����������ˮ�������������ϼ��ͷ���� | |
| D�� | �Ȼ�����ǿ����ʣ��ɵ����ˮ��Һ��ý����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
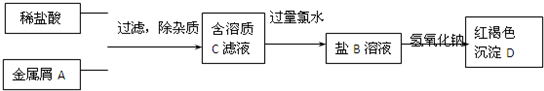
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.25L | B�� | 0.5L | C�� | 0.75L | D�� | 1L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com