
科目:高中化学 来源:不详 题型:填空题
 2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定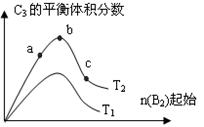
 00℃时充分反应,达平衡后C3的浓度为
00℃时充分反应,达平衡后C3的浓度为 衡后,吸收热量Q3
衡后,吸收热量Q3 kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3之间满足何种关系 (用代数式表示)。
kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3之间满足何种关系 (用代数式表示)。 器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。
器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(△H<0),把N2和H2以1︰1的物质的量之比混匀后分成两等份,同时分别充入A体积和B体积两个装有催化剂的真空容器中(A、B两容器容积固定),在保持同温度下,A、B两个容器的合成氨反应先后达到平衡状态。请回答:
2NH3(△H<0),把N2和H2以1︰1的物质的量之比混匀后分成两等份,同时分别充入A体积和B体积两个装有催化剂的真空容器中(A、B两容器容积固定),在保持同温度下,A、B两个容器的合成氨反应先后达到平衡状态。请回答: _KB(填“>”、“<”或“=”)。
_KB(填“>”、“<”或“=”)。 施为__________。
施为__________。 时混合物的平均相对分子质量]:达平衡时,容器A中N2的转化率为___________,容器B中M(平)为__________,容器______(填“A”或“B”)中,NH3的物质的量所占
时混合物的平均相对分子质量]:达平衡时,容器A中N2的转化率为___________,容器B中M(平)为__________,容器______(填“A”或“B”)中,NH3的物质的量所占 的比例较大。
的比例较大。
| | 容器A | 容器B |
| M(平) | 20 | |
| 平衡时N2的转化率 | | 10% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
2NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:  | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
| A.向混合气体中再通入N2O4 | B.保持容积不变,通入He |
| C.使用高效催化剂 | D.降低温度 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g)。下列叙述能够说明反应已达平衡状态的是
2HI(g)。下列叙述能够说明反应已达平衡状态的是| A.各物质的物质的量浓度比为1:1:2 | B.v(H2)正==v(HI)逆 |
| C.断裂2mol H-I键的同时生成1mol I-I键 | D.混合气体的颜色不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 在密闭容器中反应,达到平衡状态的标志是( )
在密闭容器中反应,达到平衡状态的标志是( )| A.NO2全部变成了NO和O2 | B.反应已经停止了 |
C.用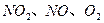 的物质的量浓度变化表示的反应速率的比为2:2:1的状态 的物质的量浓度变化表示的反应速率的比为2:2:1的状态 | |
D.单位时间内生成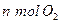 的同时生成 的同时生成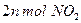 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
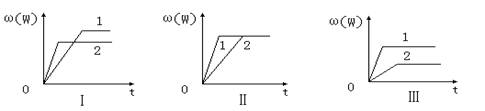
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b>n |
| B.图Ⅱ可能是同温同压催化剂对反应的影响,且1的催化剂效果更好 |
| C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 HX(g)的平衡常数为9。若将2.0 mol
HX(g)的平衡常数为9。若将2.0 mol| A.9% | B.18% | C.30% | D.80% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )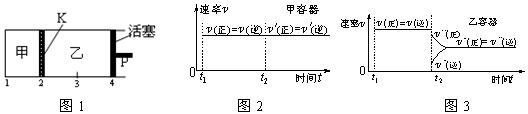
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com