
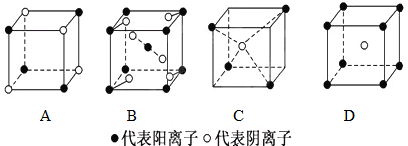
分析 (1)根据微粒所在晶胞位置,利用均摊法计算微粒数目之比,得到化学式;
(2)①根据FeS2晶体的晶体结构可知,晶体中阳离子与阴离子个数比为为1:1,所以晶体中存在亚铁离子与S22-,据此判断化学键;
②晶体结构A中相邻的阴、阳离子间的距离为a cm,所以晶胞的体积为a3cm3,晶胞中含有阴阳离子个数都是$\frac{1}{2}$,根据$ρ=\frac{m}{V}$计算密度;
解答 解:(1)A、M位于顶点,数目为4×$\frac{1}{8}$=$\frac{1}{2}$,N位于顶点,数目为4×$\frac{1}{8}$=$\frac{1}{2}$,微粒数目为1:1,即化学式为MN;
B、M分别位于晶胞的体心和顶点位置,体心占1个,顶点占8×$\frac{1}{8}$=1个,共2个,N分别位于面上和体内,面上4×$\frac{1}{2}$=2个,体内2个,共4个,即晶胞中两种微粒数目之比为1:2,化学式为MN2;
C、M位于顶点,数目为4×$\frac{1}{8}$=$\frac{1}{2}$,N位于体心,数目为1,化学式为MN2;
D、M位于顶点,数目为8×$\frac{1}{8}$=1,N位于体心,数目为1,化学式为MN,
故答案为:MN;MN2;MN2;MN;
(2)①根据FeS2晶体的晶体结构可知,晶体中阳离子与阴离子个数比为为1:1,所以晶体中存在亚铁离子与S22-,亚铁离子与S22-之间是离子键,S22-中存在共价键,所以晶体中存离子键和共价键,
故答案为:离子键和共价键;
②晶体结构A中相邻的阴、阳离子间的距离为a cm,所以晶胞的体积为a3cm3,晶胞中含有阴阳离子个数都是$\frac{1}{2}$,所以晶体的密度为ρ=$\frac{\frac{56+64}{{N}_{A}}}{{a}^{3}}$×$\frac{1}{2}$g/cm3=$\frac{60}{{N}_{A}{a}^{3}}$g/cm3,
故答案为:$\frac{60}{{N}_{A}{a}^{3}}$;
点评 本题考查了均摊法晶胞的计算、化学键、以及晶胞密度的计算等知识,为高考热点题型,难度中等,其中晶胞的计算是该题的难点,注意物质结构知识的灵活运用.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁表面涂油漆可增强其抗腐蚀性 | |
| B. | PM2.5是指大气中直径接近2.5×10-6m的颗粒,分散在空气中形成胶体 | |
| C. | 大量燃烧煤、石油等化石燃料是造成雾霾天气的一种重要因素 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤ | C. | ①②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
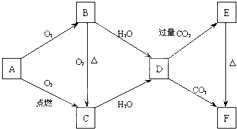 如图所示,A、B、C、D、E、F为金属钠或钠的化合物.
如图所示,A、B、C、D、E、F为金属钠或钠的化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
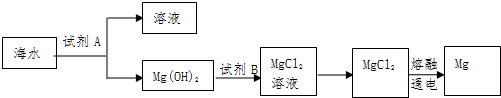
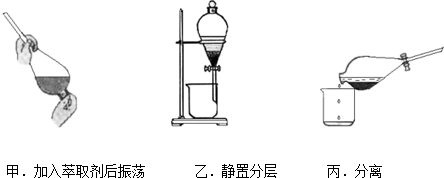
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com