
����Ŀ��һ�־��и������ȵ����ɵ��ʾ��ͼ��ͼ��ʾ��ʯī�缫�������ĵ缫��ӦΪMnO2+e��+H2O=MnO(OH)+OH-����װ�ù���ʱ������������ȷ����
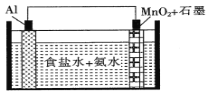
A. ʯī�缫�ϵĵ��Ʊ�Al�缫�ϵĵ�
B. Al�缫���ĵ缫��Ӧʽ��A1-3e-+3NH3��H2O=Al(OH)3+3NH4+
C. ÿ����27gAl����3mol����ͨ����Һת�Ƶ�ʯī�缫��
D. ������ʳ��ˮ+NaOH��Һ���������Һ���缫��Ӧʽ��ͬ
���𰸡�B
��������
�ŵ�ʱ�ĵ缫��Ӧʽ֮һΪMnO2+e-+H2O�TMnO(OH)+OH-��MnO2�õ��ӣ�ʯīΪ��������AlΪ������ʧ���ӣ��ڰ�ˮ��Һ��Alʧ��������Al(OH)3�����ԭ���ԭ���������
A����������������ʯīΪ������AlΪ������ʯī�缫�ϵĵ��Ʊ�Al�缫�ϵĸߣ���A����
B��MnO2�õ���Ϊ��������AlΪ������ʧ���ӣ��ڰ�ˮ��Һ��Alʧ��������Al(OH)3�������缫��ӦʽΪAl-3e-+3NH3H2O�TAl(OH)3+3NH4+����B��ȷ��
C�����ӴӸ����������������ǵ���ֻ���ڵ��ߺ͵缫���ƶ�������ͨ����Һ����C����
D��������ʳ��ˮ+NaOH��Һ���������Һ���������ɵ����������ᱻ���������ܽ⣬�缫��Ӧʽ��ͬ����D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ���仯�������ճ��������������Ź㷺��Ӧ�á���ش��������⣺
��1������Ԫ�����ڱ��е�λ����________________��
��2�������Fe(CO)x�����³�Һ̬���۵�Ϊ-20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��ж�Fe(CO)x��������___________��������ͣ���Fe(CO)x������ԭ�Ӽ۵������������ṩ������֮��Ϊ18����x=_______��Fe(CO)x��һ�������·�����Ӧ��Fe(CO)x(s)![]() Fe(s)+xCO(g)����֪��Ӧ������ֻ������λ�����ɴ��жϸ÷�Ӧ���γɵĻ�ѧ������Ϊ_________��
Fe(s)+xCO(g)����֪��Ӧ������ֻ������λ�����ɴ��жϸ÷�Ӧ���γɵĻ�ѧ������Ϊ_________��
��3��д��CO��һ�ֳ����ȵ�������ӵĽṹʽ____________��������ȽϷе�ϸߵ�Ϊ__________���ѧʽ����CN����̼ԭ���ӻ��������Ϊ__________��C��N��O��Ԫ�صĵ�һ����������Ϊ_______����Ԫ�ط��ű�ʾ����
��4��ͭ��Cl�γɻ�����ľ�����ͼ��ʾ���ڵ����ͭԭ�ӣ���
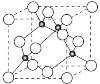
�ٸþ���Ļ�ѧʽΪ________��������Ũ���ᷢ����������ԭ��Ӧ�����������H2CuCl3����Ӧ�Ļ�ѧ����ʽΪ___________________��
����֪ͭ��M�ĵ縺�Էֱ�Ϊ1.9��3.0����ͭ��M�γɵĻ���������______������ӡ��������ۡ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ķ��ӽṹ�ɼ�д�ɼ���ʽ�ṹ![]() ���л���A�ļ���ʽ�ṹΪ
���л���A�ļ���ʽ�ṹΪ![]() ���л���B������ʵ�����H2�����ӳɷ�Ӧ�ɵõ��л���A�������й�˵��������ǣ� ��
���л���B������ʵ�����H2�����ӳɷ�Ӧ�ɵõ��л���A�������й�˵��������ǣ� ��
A. B�Ľṹ������3�֣�����һ������Ϊ2��2��3-����-2-��ϩ
B. ��ϵͳ�����������л���A������Ϊ2��2��3-��������
C. �л���A�ķ���ʽΪC8H18
D. �л���A��һ��ȡ����ֻ��5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽����Ƭ��Na2CO3��Һ�ķ�Ӧ������˵������ȷ���ǣ� ��
|
| |
���������� | ��Ƭ�������ϸС���� | ���ְ�ɫ���ǣ������������ݣ�������ΪH2��CO2�� |
A.�ԱȢ�˵��Na2CO3��Һ���ƻ�������ı���Ĥ
B.Na2CO3��Һ�д���ƽ�⣺CO32-+H2O![]() HCO3- +OH-
HCO3- +OH-
C.���Ⱥ�H2�ݳ���CO32-ˮ��ƽ���ƶ������Ӱ�����෴��
D.�Ʋ���ְ�ɫ���ǵ�ԭ��AlO2-+HCO3-+H2O=Al(OH)3��+CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��11.9g������(Sn)��100mL12mol��L��1 HNO3����һ��ʱ�䡣��ȫ��Ӧ��ⶨ��Һ��c(H��)Ϊ8 mol��L��1����Һ�����Ϊ100mL������������ȫ��������������Һ���գ�������������0.4mol���ɴ��ƶ�������������ǣ� ��
A.SnO2��4H2OB.Sn(NO3)4
C.Sn(NO3)2D.Sn(NO3)2��Sn(NO3)4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ӡˢͭ�Ƶ�·��ĸ�ʴҺѡȡ�ͻ���������һֱ���о����ȵ㡣
��1��Ӧ�ô�ͳʴ��Һ(HCl-FeCl3)
��ʴ��ͭ����Ҫ��Ӧ�����ӷ���ʽΪ_____��
�ڸ�ʴ������ͨ�����������ɷ����ͭ����ʵ��FeCl3��Һ������
![]()
����I�����Լ��Ͳ����ֱ�Ϊ______����ʵ�ֲ���IIת�������ʻ���____����һ�ּ��ɣ���
��2��Ӧ������ʴ��Һ(HCl-H2O2)��������ʴ�̷�Һ����������ͼ��
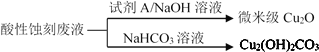
��ʴ��ͭ����Ҫ��Ӧ�����ӷ���ʽΪ_____��
�ڻ�����Cu2O�����У�������Լ�A��____������ĸ����
a.Fe�� b.������ c. NaCl���� d.����KMnO4��Һ
�ۻ���Cu2(OH)2CO3�Ĺ���������Ʒ�Ӧ���¶ȣ����¶ȸ���80��ʱ����Ʒ��ɫ��������ԭ�������_____��
��3��Ӧ�ü���ʴ��Һ(NH3H2O�CNH4Cl) ʴ��ͭ�壬����Cu(NH3)4Cl2��ˮ���ɡ�ʴ��ͭ����Ҫ��Ӧ�Ļ�ѧ����ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��������ʵ�������ȷ����
A.���������ϡ���ᷴӦ��2Fe+6H+![]() 2Fe3++3H2��
2Fe3++3H2��
B.��Ca(OH)2��NH4Cl�����Ϲ�����ȡ����������OH����NH4+![]() NH3����H2O
NH3����H2O
C.����NaOH��Һ��Ӧ��Al+2OH��= AlO2��+ H2��
D.NO2����ˮ��3NO2��H2O![]() 2H++ 2NO3��+ NO
2H++ 2NO3��+ NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2(g) + O2(g) ![]() 2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У���ȷ����
2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У���ȷ����
�� | �� | �� | ||
��ʼ���ʵ��� | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
n(O2) / mol | 0.24 | 0.24 | 0.48 | |
SO2��ƽ��ת���� / % | 80 | ��1 | ��2 | |
A. ���з�Ӧ��ƽ�ⳣ��С����
B. ƽ��ʱ������c(SO3)�Ǽ��е�2��
C. ���¶��£�ƽ�ⳣ��ֵΪ400
D. ƽ��ʱ������O2��ת���ʴ�������O2��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ����֪��Ӧ���̷��ȣ����������������ֺ���Ԫ�ص����ӣ�����ClO-��ClO3-�������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ����ͼ��ʾ������˵����ȷ���� �� ��
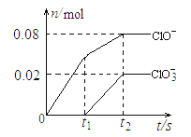
A.���Լ���Һ��KOH��������15.68 g
B.��Ӧ��ClO3������������ΪCl2ͨ�����
C.������������ ClO�� ��ClO3��������Cl2
D.һ����3.136 L�������뷴Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com