
【题目】某分子的球棍模型如下图所示,图中“棍”代表单键或双键或三键;不同颜色的球代表不同元素的原子。有关该分子的说法错误的是:
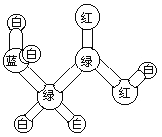
A. 不属于烃类 B. 能发生聚合反应
C. 不能与盐酸反应 D. 能与金属钠发生置换反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】水是生命之源,是一切生命活动的基础。下列有关水的说法不正确的是( )
A. 水可以参与细胞中的化学反应
B. 细胞内的许多化学反应需要有水参与
C. 种子入库前晒干的目的是减少种子体内的自由水和结合水
D. 自由水与结合水比值降低,会影响细胞的代谢活动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是
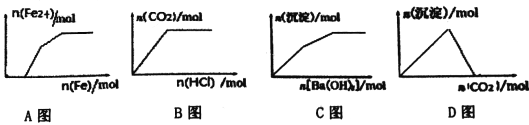
A. Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉
B. Na2CO3、NaHCO3溶液中逐滴加入HCl
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液
D. NaAlO2溶液中逐渐通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为_________
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤
步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。
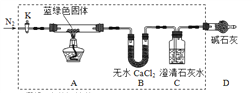
请回答下列问题:
(1)假设2中的沉淀为___________________。
(2)假设1中沉淀为Cu(OH)2的理论依据是(用离子方程式表示)____________。
(3)无水乙醇洗涤的目的_______________________________________。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明___________成立。(填写“假设1” “假设2”或“假设3”)。
(5)乙同学认为只要将上图中B装置的试剂改用______试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
A. 浓硫酸的体积增大
B. 铝的表面生成致密的氧化膜
C. 澄清的石灰水变浑浊
D. 氢氧化钠的表面发生潮解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在恒温条件下,将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
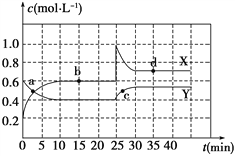
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):____________________。
(2)0~10min化学反应速度V(X)=__________________。
(3)比较Y在0~10min和10~20min时平均反应速率的大小:v(0~10)_______ v(10~20)(填“<”、“>”或“=”),原因是________________。
(4) a、b、c、d四个点中,表示化学反应处于平衡状态的点是_________,理由是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生存和发展的重要支柱,碳元素的单质及化合物是人类生产生活的主要能源物质.
(1)有机物M经过太阳光光照可转化为N,转化过程如下: 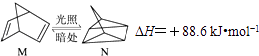
则M、N相比,较稳定的是 .
(2)CO可用于合成燃料甲醇.在有催化剂存在的10L恒容密闭容器中充入2mol CO和4mol H2 , 发生如下反应:CO(g)+2H2(g)CH3OH(g). 测得CO的平衡转化率与温度、压强的关系如图所示:
①判断上述反应达到平衡状态的依据是(填字母编号).
A.CH3OH的生成速率与CO的消耗速率相等
B.CH3OH、CO、H2的浓度都不再发生变化
C.混合气体的密度不变
D.混合气体的相对平均分子质量不变
②下列措施中,能使上述平衡体系中 ![]() 的值增大的是(填字母编号).
的值增大的是(填字母编号).
A.降低温度 B.充入He(g),使体系压强增大 C.再充入1mol CO和2mol H2
③100℃时反应在5min末达到平衡,则从反应开始至达平衡,v(H2)=mol/(Lmin);该温度下反应的平衡常数K= . 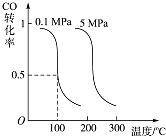
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下图中氮元素及其化合物的转化关系,回答问题:
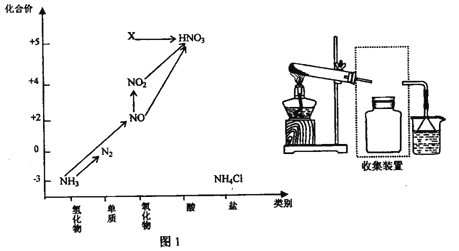
(1)实验窒常用NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为___________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图。___________
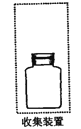
(3)下列试剂不能用手干燥NH3的是_________。
A.浓硫酸 B.碱石灰 C.NaOH 固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO 化学方程式为____________。
②NO→NO2 实验现象是_______ 。
③ NO2![]() HNO3 氧 化剂 与 还原剂物质的量之比为_______。
HNO3 氧 化剂 与 还原剂物质的量之比为_______。
(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,则该物质的化学式为_____________,
(6) 图1中,X的化学式为__________,从物质性质上看,X 属于_______氧化物。
(7)若要将NH3→N2,,从原理上看,下列试剂可行的是_______。
A.O2 B.Na C.NH4Cl D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的决定因素是______
A.元素原子半径大小呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com