
| A. | 纯碱溶液清洗油污,加热可增强其去污能力 | |
| B. | 门窗玻璃、陶瓷餐具、玛瑙手镯、砖瓦所用材料为硅酸盐材料 | |
| C. | 聚丙烯酸钠是一种高吸水性树脂 | |
| D. | 汽油、煤油、植物油都是油,但它们的主要成分不相同 |
分析 A、加热促进碳酸根的水解,碱性增强,去污效果好;
B、水晶和玛瑙的主要成分是二氧化硅;
C、根据聚丙烯酸钠的性质来回答判断;
D、汽油、煤油、植物油的成分不同.
解答 解:A、纯碱是碳酸钠的水溶液,碳酸根离子水解显示碱性,加热促进碳酸根的水解,碱性增强,去污效果好,故A正确;
B、水晶和玛瑙的主要成分是二氧化硅,不是硅酸盐,即玛瑙手镯所用材料不是硅酸盐材料,故B错误;
C、聚丙烯酸钠树脂是一种高吸水性的材料,故C正确;
D、汽油、煤油是烃类的混合物,植物油是酯类,成分不同,故D正确.
故选B.
点评 本题涉及物质的成分、物质的性质应用以及盐的水解平衡的移动等知识,属于综合知识的考查,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
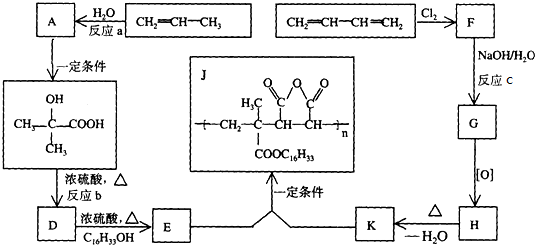
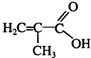 +C16H33OH$→_{△}^{浓硫酸}$
+C16H33OH$→_{△}^{浓硫酸}$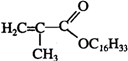 +H2OE+K→J
+H2OE+K→J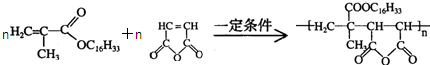
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 操作 | 现象 | 结论 |
| A | Al2(SO4)3溶液中滴加过量Ba(OH)2 | 生成白色沉淀物 | Al(OH)3不溶于Ba(OH)2 |
| B | 铜与浓硝酸反应,生成气体用湿润KI-淀粉试纸检验 | 试纸变蓝 | NO2具有氧化性 |
| C | 向溶液中滴加盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 该溶液中可能含有SO42- |
| D | 向CuCl2和MgCl2混合溶液中加入过量的NaOH溶液 | 产生蓝色沉淀 | NaOH不和MgCl2反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
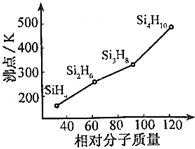 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定浓度的氨水加水稀释的过程中,$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的比值增大 | |
| B. | 假设HClO的电离平衡常数为Ka,碳酸的电离常数分别记为:Ka1 和Ka2,已知:Ka1>Ka>Ka2,则发生反应:2NaClO+CO2(少量)+H2O=Na2CO3+2HClO | |
| C. | 等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+) | |
| D. | 室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的非金属性强于W,所以X的氢化物沸点高于W的氢化物沸点 | |
| B. | Y、Z均为金属元素,故X、Y、Z三种元素不能形成化合物 | |
| C. | 工业上常利用电解ZW3溶液冶炼金属Z | |
| D. | Y、W的最高价氧化物水化物均能溶解Z单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| B. | 1molCl2与足量Fe反应转移电子数一定为3NA | |
| C. | 1mol氨基(-NH2)中含电子数为10nA | |
| D. | 标况下,11.2LSO3所含的分子数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
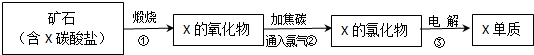
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com