
常温下,下列各组离子在指定溶液中一定能大量共存的是(双选)( )
A.1.0 mol·L-1的KNO3溶液:NH 、Fe2+、Cl-、SO
、Fe2+、Cl-、SO
B.1.0 mol·L-1的NaAlO2溶液:Cl-、HCO 、K+、Ba2+
、K+、Ba2+
C.1.0 mol·L-1的FeCl2溶液:NO 、Na+、K+、ClO-
、Na+、K+、ClO-
D.澄清透明的溶液:Cu2+、SO 、Mg2+、Cl-
、Mg2+、Cl-
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
①用一种试剂将下列各组物质鉴别开.
(1) 和
和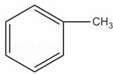 :
:
(2) ,
, 和C6H12(已烯):
和C6H12(已烯):
(3)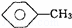 ,CCl4和乙醇
,CCl4和乙醇
②填写
(1)CH3COOC2H5中含有官能团的名称:
(2)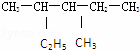 的系统命名:
的系统命名:
(3)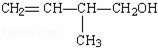 的键线式: .
的键线式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y 处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素X不能与元素Y形成化合物X2Y2
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物的水化物都是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
有一混合溶液,只可能含有以下离子中的若干种:K+、NH 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO 、SO
、SO ,现取三份100 mL溶液进行如下实验:
,现取三份100 mL溶液进行如下实验:
(1)向第一份溶液中加入AgNO3溶液有沉淀产生;
(2)向第二份溶液中加入足量NaOH溶液加热后,收集到气体0.06 mol;
(3)向第三份溶液中加入足量BaCl2溶液后,所得沉淀经洗涤、干燥后,质量为6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是(双选)( )
A.K+一定存在 B.100 mL溶液中含0.02 mol CO
C.Cl-可能存在 D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
在下述条件下,一定能大量共存的离子组是( )
A.无色透明的水溶液中:K+、Ba2+、Cl-、MnO
B.含有大量NO 的水溶液中:NH
的水溶液中:NH 、Fe2+、SO
、Fe2+、SO 、H+
、H+
C.滴入酚酞试剂显红色的溶液中:Na+、K+、CO 、Br-
、Br-
D.强碱性溶液中:ClO-、S2-、HSO 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对各组离子或物质是否能够大量共存解释正确的是(双选)( )
| A | 常温常压下NH3、O2、H2、CO2 | 不能 |
| 共存 | NH3为碱性气体、CO2为酸性气体,二者反应生成(NH4)2CO3 | |
| B | c(OH-)=1.0×10-13 mol·L-1溶液中,Fe2+、NO | 不能 |
| 共存 | 发生反应:3Fe2++NO | |
| C | 溶液中:K+、Cu2+、Cl-、NH3·H2O | 不能 |
| 共存 | 发生反应:Cu2++2NH3·H2O===Cu(OH)2↓+2NH | |
| D | 溶液中:Al3+、Na+、SO | 可以 |
| 共存 | 不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数的数值约为6.02×1023,下列叙述中正确的是( )
A.0.5 g C3H4中含有共用电子对的数目为0.1×6.02×1023
B.3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1×6.02×1023
C.25℃时,pH=1的醋酸溶液中含有H+的数目为0.1×6.02×1023
D.标准状况下,2.24 L CHCl3中含有的分子数为0.1×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是( )
| 选项 | 事实 | 结论 |
| A | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| B | HCl与Na2CO3溶液反应生成CO2 | 可用饱和Na2CO3溶液除去CO2中的少量HCl |
| C | 氧化铜高温下生成红色物质,该物质可与稀硫酸反应 | 氧化铜高温下可分解生成Cu2O |
| D | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒压密闭容器M(如图Ⅰ) 和恒容密闭容器N(如图Ⅱ)中,分别加入a molA和a molB,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?) + B(?) xC(g) ΔH<0
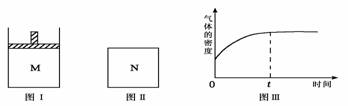 平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断正确的是( )
平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断正确的是( )
A. x =4
B. 若N中气体的密度如图Ⅲ所示,则A、B一定都是气态
C. 若A为气体,B为非气体,则平衡时M、N中C的物质的量相等
D. 若A、B均为气体,平衡时M中A的转化率小于N中A的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com