
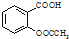
 ����������Ӧ����㷺�Ľ��ȡ���ʹ�Ϳ���ҩ������ˮ���������ֽ⣬�ֽ��¶�Ϊ128��135�森ijѧϰС����ʵ������ˮ���ᣨ���ǻ������ᣩ�������[��CH3CO��2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣��Ʊ����������������£�
����������Ӧ����㷺�Ľ��ȡ���ʹ�Ϳ���ҩ������ˮ���������ֽ⣬�ֽ��¶�Ϊ128��135�森ijѧϰС����ʵ������ˮ���ᣨ���ǻ������ᣩ�������[��CH3CO��2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣��Ʊ����������������£�
| ���� | ��Է������� | �۵��е� ���棩 | ˮ |
| ˮ���� | 138 | 158���۵㣩 | �� |
| ������ | 102 | 139.4���е㣩 | ��Ӧ |
| ��ϩˮ���� | 180 | 135���۵㣩 | �� |


���� ��1��������������ˮ�⣬������Ӧ���
��2�������¶���85�桫90�棬�¶ȵ���100�棬Ӧ��ȡˮԡ���ȣ�
��3������ˮ����Ϊ����ˮ�����ʣ�������֮�����ת��Ϊ������ˮ���Σ����벻�������ʷ��룻
��4�������ڼ���ʱ�¶Ȳ��ܹ��ߣ�Ӧ������һ����Χ֮�ڣ���ʹ���¶ȼƣ�����ˮ����Ϊ���½��ϳ�����
��ˮ���������������������ﵽ�����Ŀ�ģ�
��5��ˮ���Ậ�з��ǻ������Ȼ�����Һ����ɫ���ݴ���Ƽ�������Ʒ���Ƿ����ˮ���
��6������������������ˮ������������ɼ�������ʣ�
��� �⣺��1��������������ˮ���������ᣬ������Ӧ�����ֹ������ˮ�⣬
�ʴ�Ϊ����ֹ������ˮ�⣻
��2�������¶���85�桫90�棬С��100�棬Ӧʹ��ˮԡ���ȣ�
�ʴ�Ϊ��ˮԡ���ȣ�
��3������ˮ����Ϊ����ˮ�����ʣ�������֮�����ʹ����ˮ������NaHCO3��Һ����ת��Ϊ������ˮ������ˮ�����ƣ�������ۺ�����룬
�ʴ�Ϊ��ʹ����ˮ������NaHCO3��Һ����ת��Ϊ������ˮ������ˮ�����ƣ�������ۺ�����룻
��4���ټ���ʱ�¶Ȳ��ܹ��ߣ�Ӧ������һ����Χ֮�ڣ������¶ȼƿ����¶ȣ���ֹ����ˮ�������ȷֽ⣬Ϊ�������������ˮ������������Ӧ���¶˽����϶˳���
�ʴ�Ϊ�����Ʒ�Ӧ�¶ȣ���ֹ�¶ȹ��ߣ�����ˮ�������ȷֽ⣻b��
��ˮ��������������������������ˮ����������������������ʹ���߳�ַ��룬
�ʴ�Ϊ��ˮ����������������������ȴ�ᾧʱ���ܽ������������У����ٽᾧ������
��5��ˮ���Ậ�з��ǻ������Ȼ�����Һ����ɫ�����巽��Ϊ����ˮ�м���������Ʒ��Ȼ��μ�FeCl3��Һ��������ɫ���֣�˵����Ʒ����ˮ���������ɫ���֣�˵����Ʒ�в���ˮ���ᣬ
�ʴ�Ϊ��ˮ����������������������ȴ�ᾧʱ��ˮ�������ܽ������������к��ٽᾧ������
��6��n��ˮ���ᣩ=$\frac{2.0g}{138g/mol}$=0.0145mol��n����������=$\frac{5.0mL��1.08g/mL}{102g/mol}$=0.053mol������������������ˮ����0.0145mol������Ϊ$\frac{2.2g}{0.0145mol��180g/mol}$=84.3%��
�ʴ�Ϊ��84.3%��
���� ���⿼���л���ϳɵķ�����������ۣ���Ŀ�Ѷ��еȣ�����ע�����ʵ�����ԭ�������������Ϣ������ʵ�����������ѧϰ��ע����ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 9a/b mol-1 | B�� | 9b/a 1mol-1 | C�� | b/a mol-1 | D�� | a/bmol- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 11.7g | B�� | 5.85g | C�� | 8g | D�� | 15.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | 2 | C�� | 3 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����в����ڶ����ġ����ӡ� | |
| B�� | ̼ԭ�Ӽ��Թ��ۼ����� | |
| C�� | ��Ӳ����������֮һ | |
| D�� | ��ѧ�����ȶ�����ʹ�ڸ�����Ҳ����������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com