
���� ��1����Щ���Ϸ�Ӧ�����ȷ�Ӧ����̼�Ͷ�����̼��Ӧ��һ����̼��������ֽⷴӦ�����ȷ�Ӧ��
��2�������������������е������������ࣻ
��3�������к��ȵĸ�����ǿ��ǿ���ϡ��Һ��ȫ��Ӧ����1molˮ�ų�������������
��4�����ݾɼ��������յ�������ȥ�¼������ͷŵ�����ֵ��Ϊ��Ӧ�Ƚ��ȼ�շ�ӦΪ���ȷ�Ӧ��
��� �⣺��1���γɻ�ѧ����ȼ�ϵ�ȼ�ա�����кͷ�Ӧ��ըҩ�ı�ը���̶����ڷ��ȷ�Ӧ�������Ϸ�Ӧ��һ��Ϊ���ȷ�Ӧ���������̼��C�ķ�Ӧ�������ȷ�Ӧ�����Բ�һ���ͷ�������Ϊ��������ֽⷴӦ�����ȷ�Ӧ����̼��Ʒֽ⣬
�ʴ�Ϊ��AB��
��2�������������������������Ƚϣ����������е������࣬�����ȫȼ���������ų��������࣬
�ʴ�Ϊ��A��
��3��1mol H2SO4��NaOH��Һǡ����ȫ��Ӧʱ����2molH2O���ų�QkJ�������к���ָ����1molˮ�ų�����������H2SO4��NaOH��Ӧ���к���Ϊ��$\frac{Q}{2}$kJ/mol��
�ʴ�Ϊ��$\frac{Q}{2}$��
��4��1molH2O�к�2molH-O�����Ͽ�1molH-H��1molO=O��1molO-H�������յ������ֱ�ΪQ1��Q2��Q3kJ�����1molO-H���ų�Q3kJ���������ڷ�ӦH2��g��+$\frac{1}{2}$O2��g��=H2O��g�����Ͽ�1 mol O=O����1 molH-O�������յ�����Q1+$\frac{1}{2}$Q2�������¼��ͷŵ�����2Q3���÷�Ӧ���ȣ�2Q3-��Q1+$\frac{1}{2}$Q2����0����2Q1+Q2��2Q3��
�ʴ�Ϊ��C��
���� ���⿼���˻�ѧ��Ӧ�������仯��ע�������к��ȵĸ����4��1molH2O�к�2molH-O��Ϊ����״��㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��D2 | B�� | T2O��H2O | ||
| C�� | ${\;}_{19}^{40}$K��${\;}_{19}^{39}$K | D�� | ���ʯ��ʯī |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
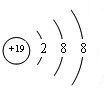 ��Ԫ�آ�����Ϊ�壬�����ڱ��е�λ���ǵ������ڢ�A�壮
��Ԫ�آ�����Ϊ�壬�����ڱ��е�λ���ǵ������ڢ�A�壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�������ˮ | B�� | �Ȼ�������ˮ | C�� | �ɱ����� | D�� | ���ȷֽ��Ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѡ��������Ǧ��Ĺ������ڻ�ѧ�仯 | |
| B�� | ��Ǧ���շ�Ӧ�У�PbS�ǻ�ԭ������ԭ����ֻ��PbO | |
| C�� | ��1molPbSұ����Pb������������Ҫ6g̼ | |
| D�� | ����ұ�������У���ȡ1molPb��ת��2mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ú������õ���ú���ͣ����пɷ���������ױ������ױ����л������� | |
| B�� | 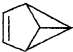 ��һ�ȴ�����3�� ��һ�ȴ�����3�� | |
| C�� | �����ֶ��Ļ�Ϊͬ���칹�壬����ߵ�ˮ�����һ������ͬ | |
| D�� | ľ�Ǵ���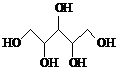 ���������ǣ� ���������ǣ�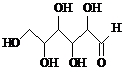 ������Ϊͬϵ����������� ������Ϊͬϵ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӿ����з��Ӽ�������Խ����Խ�ȶ� | |
| B�� | ������������ˮʱֻ�ƻ����Ӽ� | |
| C�� | ���������ӵľ�����һ���������� | |
| D�� | 1 mol�������辧�庬4 mol Si-O�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com