
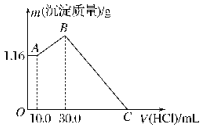
 °ŃNaOH”¢MgCl2”¢AlCl3ČżÖÖ¹ĢĢå×é³ÉµÄ»ģŗĻĪļČÜÓŚ×ćĮæĖ®ŗ󣬲śÉś1.16g°×É«³Įµķ£¬ŌŁĻņĖłµĆČÜŅŗÖŠÖšµĪ¼ÓČė1.00mol•L-1HClČÜŅŗ£¬¼ÓČėHClČÜŅŗµÄĢå»żÓėÉś³É³ĮµķµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ŹŌ»Ų“š£ŗ
°ŃNaOH”¢MgCl2”¢AlCl3ČżÖÖ¹ĢĢå×é³ÉµÄ»ģŗĻĪļČÜÓŚ×ćĮæĖ®ŗ󣬲śÉś1.16g°×É«³Įµķ£¬ŌŁĻņĖłµĆČÜŅŗÖŠÖšµĪ¼ÓČė1.00mol•L-1HClČÜŅŗ£¬¼ÓČėHClČÜŅŗµÄĢå»żÓėÉś³É³ĮµķµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ŹŌ»Ų“š£ŗ·ÖĪö ĻņĖ®ÖŠ¹ĢĢå×é³ÉµÄ»ģŗĻĪļČÜŅŗÖŠ¼ÓČėŃĪĖįŹ±£¬0-AŹ±Ć»ÓŠ³ĮµķÉś³É£¬ĖµĆ÷ČÜŅŗÖŠNaOH¹żĮ棬ŌņĀĮĄė×ÓĶźČ«×Ŗ»ÆĪŖĘ«ĀĮĖįøłĄė×Ó£¬ČÜŅŗÖŠ“ęŌŚµÄ³ĮµķĪŖMg£ØOH£©2£»
A-B¶Ī£¬ŃĪĖįŗĶĘ«ĀĮĖįÄĘ·“Ӧɜ³ÉĒāŃõ»ÆĀĮ³Įµķ£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖH2O+AlO2-+H+=Al£ØOH£©3”ż£¬BµćČÜŅŗÖŠ“ęŌŚµÄČÜÖŹŹĒĀČ»ÆÄĘ£¬³ĮµķĪŖMg£ØOH£©2”¢Al£ØOH£©3£»
B-C¹ż³ĢÖŠ£¬ĒāŃõ»ÆĆ¾ŗĶĒāŃõ»ÆĀĮ¶¼ÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆĀĮŗĶĀČ»ÆĆ¾£¬ĖłŅŌCµćČÜŅŗÖŠµÄČÜÖŹŹĒĀČ»ÆĀĮ”¢ĀČ»ÆĆ¾ŗĶĀČ»ÆÄĘ£®
½ā“š ½ā£ŗ£Ø1£©ĻņĖ®ÖŠ¹ĢĢå×é³ÉµÄ»ģŗĻĪļČÜŅŗÖŠ¼ÓČėŃĪĖįŹ±£¬0-AŹ±Ć»ÓŠ³ĮµķÉś³É£¬ĖµĆ÷¼ÓČė10.0 mLŃĪĖįÕżŗĆÖŠŗĶ¹żĮæµÄNaOH£¬ŌŁ¼ÓŃĪĖį³ĮµķŌö¼Ó£¬ĖµĆ÷AlO${\;}_{2}^{-}$×Ŗ»ÆĪŖAl£ØOH£©3£¬¹ŹAµć³ĮµķĪŖMg£ØOH£©2£¬
¹Ź“š°ø£ŗMg£ØOH£©2£» ¼ÓČė10.0 mLŃĪĖįÕżŗĆÖŠŗĶ¹żĮæµÄNaOH£¬ŌŁ¼ÓŃĪĖį³ĮµķŌö¼Ó£¬ĖµĆ÷AlO${\;}_{2}^{-}$×Ŗ»ÆĪŖAl£ØOH£©3£¬¹ŹAµć³ĮµķĪŖMg£ØOH£©2£»
£Ø2£©A-B¶Ī£¬ŃĪĖįŗĶĘ«ĀĮĖįÄĘ·“Ӧɜ³ÉĒāŃõ»ÆĀĮ³Įµķ£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖH2O+AlO2-+H+=Al£ØOH£©3”ż£¬
¹Ź“š°ø£ŗH2O+AlO2-+H+=Al£ØOH£©3”ż£»
£Ø3£©A-B¶Ī£¬ŃĪĖįŗĶĘ«ĀĮĖįÄĘ·“Ӧɜ³ÉĒāŃõ»ÆĀĮ³Įµķ£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖH2O+AlO2-+H+=Al£ØOH£©3”ż£¬øł¾ŻHClµÄĢå»żÖŖ£¬n£ØAlO2-£©=n£ØHCl£©=1mol/L”Į£Ø0.03-0.01£©L=0.02mol£¬ĀČ»ÆĀĮµÄÖŹĮæ=0.02mol”Į133.5g/mol=2.67g£»
¹Ź“š°øĪŖ£ŗ2.67£»
£Ø4£©øł¾ŻĀĮŌ×ÓŹŲŗćµĆn£ØAlCl3£©=n£ØAlO2-£©=0.02mol£¬ÓÉNa+Ąė×ÓŗĶCl-Ąė×ÓŹŲŗćµĆ£¬Ō»ģŗĻĪļÖŠn£ØNaOH£©=n£ØNaCl£©=n£ØCl-£©=2n£ØMgCl2£©+3n£ØAlCl3£©+n£ØHCl£©=0.02mol”Į2+0.02mol”Į3+0.03L”Į1mol/L=0.13mol£¬CµćČÜŅŗĪŖMgCl2”¢AlCl3ŗĶNaCl»ģŗĻŅŗ£¬CµćĖł¼ÓŃĪĖįÓĆÓŚÖŠŗĶŌ»ģŗĻĪļÖŠµÄNaOH£¬“ĖŹ±Ėł¼ÓŃĪĖįĪļÖŹµÄĮæ£ŗ
n£ØHCl£©=n£ØNaOH£©=0.13mol£»PµćĖł±ķŹ¾ŃĪĖįµÄĢå»żĪŖ£ŗV=$\frac{0.13mol}{1mol/L}$=0.13L=130ml£¬
¹Ź“š°øĪŖ£ŗ130£®
µćĘĄ ¶ŌÓŚĶ¼Ļó·ÖĪöĢāµÄ½āĢā¹ęĀÉ£ŗŅŖĆ÷Č·ĆæŅ»¶ĪĶ¼Ļó·¢ÉśµÄ»Æѧ·“Ó¦”¢ÖŖµĄ¹Õµć“ś±ķµÄŗ¬Ņå¼°ČÜŅŗÖŠČÜÖŹµÄ³É·Ö£¬½įŗĻ·½³ĢŹ½¶ŌÓŠ¹ŲĪŹĢā½ųŠŠ·ÖĪö£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«Ćŗ·ŪĖéŗóČ¼ÉÕ | B£® | ĶØČė“óĮæµÄæÕĘų | ||
| C£® | ¼ÓČėµÄĆŗŌ½¶ąŌ½ŗĆ | D£® | ½«ĆŗŗĶæÕĘųŌŚĆܱյÄæÕ¼äĄļČ¼ÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŌŖĖŲ | Ō×Ó½į¹¹»ņŠŌÖŹ |
| A | ĘäŠĪ³ÉµÄŅ»ÖÖĶ¬Ī»ĖŲŌŖĖŲŌŚæ¼¹ÅÖŠæÉĶĘ²ā»ÆŹÆµÄÄź“ś |
| B | ÓėAĶ¬ÖÜĘŚ£¬Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĪŽĀŪÅØ”¢Ļ”ČÜŅŗ¾łÓŠĒæŃõ»ÆŠŌ |
| C | µŲæĒÖŠŗ¬Įæ×ī¶ąµÄŌŖĖŲ |
| D | DŌ×ÓµÄ×īĶā²ćµē×ÓŹżÓėĘäµē×Ó²ćŹżĻąĶ¬£¬ŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲ |
| E | Ę䵄֏Ö÷ŅŖ“ęŌŚÓŚ»šÉ½æŚø½½ü |
| F | Éś»īÖŠ³£¼ūµÄ½šŹō£¬ĖüµÄijÖÖŃõ»ÆĪļ¾łÓŠ“ÅŠŌ |
| G | GŌ×ÓÓėDŌ×ÓĶ¬ÖÜĘŚ£¬ĒŅŌ×Ó°ė¾¶ŹĒĶ¬ÖÜĘŚŌŖĖŲÖŠ×ī“óµÄ |
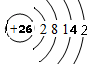 £»
£» £¬
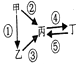
£¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{1}{14}$ mol•L-1 | B£® | $\frac{4}{5}$ mol•L-1 | C£® | $\frac{1}{28}$ mol•L-1 | D£® | $\frac{1}{42}$ mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1LøĆČÜŅŗÖŠŗ¬KNO3101g | |
| B£® | 100 mLøĆČÜŅŗÖŠŗ¬KNO3 0.01mol | |
| C£® | “Ó1LøĆČÜŅŗÖŠČ”³ö500 mLŗó£¬Ź£ÓąČÜŅŗµÄÅضČĪŖ0.05 mol/L | |
| D£® | 1LĖ®ÖŠČܽā0.1 mol KNO3£¬¼“æÉÅäµĆ0.1 mol/L KNO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
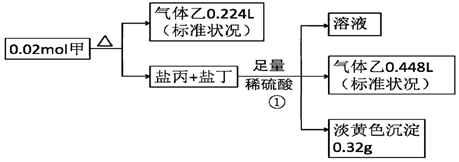
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| ŌŖĖŲ | Ļą ¹Ų ŠÅ Ļ¢ |
| A | Ō×ÓŗĖĶāÓŠ7ÖÖŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó |
| B | ĶāĪ§µē×ÓÅŲ¼Ź½ĪŖnsnnpn+2 |
| C | ³£¼ūµÄ½šŹō£¬ŌŚÖÜĘŚ±ķÖŠÖÜĘŚŠņŹżÓė×åŠņŹżĻąµČ |
| D | ĘųĢ¬Ēā»ÆĪļ¼°×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ¾łĪŖĒæĖį |
| E | Ņ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ56£¬ÖŠ×ÓŹżĪŖ30 |
| F | µ„ÖŹ×ĻŗģÉ«£¬µēĄĀ²ÄĮĻ£¬³£¼ūŃõ»ÆĪļĪŖŗŚÉ« |
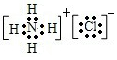
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·Ö×ÓŹ½ | ½į¹¹¼ņŹ½ | Ķā¹Ū | ČŪµć | ČܽāŠŌ |
| C12H10ClN3O | 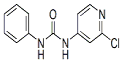 | °×É«½į¾§·ŪÄ© | 170”«172”ćC | Ņ×ČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com