
| A. | 氯化亚铁溶液中加入双氧水 | |
| B. | 硫酸亚铁酸性溶液中滴加硝酸钾溶液 | |
| C. | 硫酸铜溶液中滴加硝酸钡溶液 | |
| D. | 高锰酸钾酸性溶液中滴加亚硫酸钠溶液 |
分析 A、氯化亚铁溶液中加入双氧水,亚铁离子与双氧水发生氧化还原反应,亚铁离子转化为铁离子;
B、硫酸亚铁酸性溶液中滴加硝酸钾溶液,亚铁离子与氢离子和硝酸根离子发生氧化还原反应,亚铁离子转化为铁离子;
C、硫酸铜溶液和硝酸钡溶液之间会发生反应生成硫酸钡白色沉淀和硝酸铜;
D、高锰酸钾与亚硫酸钠发生氧化还原反应.
解答 解:A、氯化亚铁溶液中加入双氧水,亚铁离子与双氧水发生氧化还原反应,亚铁离子转化为铁离子,颜色由浅绿色变成黄色,故A不选;
B、硫酸亚铁酸性溶液中滴加硝酸钾溶液,亚铁离子与氢离子和硝酸根离子发生氧化还原反应,亚铁离子转化为铁离子,颜色由浅绿色变成黄色,故B不选;
C、硫酸铜溶液和硝酸钡溶液之间会发生反应生成硫酸钡白色沉淀和硝酸铜,溶液颜色仍是蓝色,故C选;
D、高锰酸钾与亚硫酸钠发生氧化还原反应,溶液变为无色,故D不选;
故选C.
点评 本题考查较为综合,涉及物质的颜色的变化,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
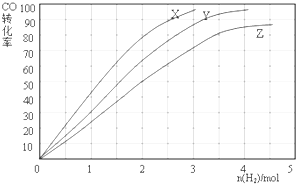
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
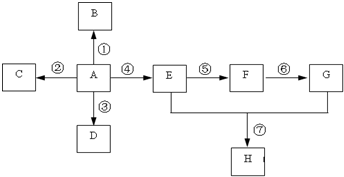 已知A是一种重要的基本化工原料,其分子中碳元素的百分含量为85.7%,且相对分子量小于30.A、B、C、D、E、F、G、H有下图所示的转化关系(部分产物已略去).其中B为高分子化合物,C为无色无味气体,实验室中可以通过G与大理石制取.D为烃,不能使酸性高锰酸钾溶液褪色.E、G为生活中常见的有机物,且E有特殊香味,H有香味.
已知A是一种重要的基本化工原料,其分子中碳元素的百分含量为85.7%,且相对分子量小于30.A、B、C、D、E、F、G、H有下图所示的转化关系(部分产物已略去).其中B为高分子化合物,C为无色无味气体,实验室中可以通过G与大理石制取.D为烃,不能使酸性高锰酸钾溶液褪色.E、G为生活中常见的有机物,且E有特殊香味,H有香味.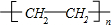 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
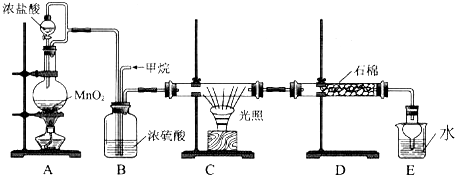
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.005mol | B. | 0.01mol | C. | 0.015mol | D. | 0.02mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基戊烷 | ||
| C. | 3-甲基-2-乙基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com