
下列说法不正确的是( )
A.Ksp只与难溶电解质的性质和温度有关
B.由于Ksp(ZnS)>Ksp(CuS),所以ZnS在一定条件下可转化为CuS
C.其他条件不变,离子浓度改变时,Ksp不变
D.两种难溶电解质作比较时,Ksp越小的电解质,其溶解度一定越小
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某恒温密闭容器中,可逆反应A(s)B+C(g) ΔH=+Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是( )
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)反应∶n(C)生成=1∶1
C.若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q kJ
D.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
“嫦娥一号”探月卫星的成功发射,标志着我国的空间探究已进入一个新的阶段。“嫦娥一号”的研制,应用了许多尖端的合成高分子材料。高分子材料与一般金属材料相比,其优越性是 ( )。
①强度大 ②溶解性好 ③电绝缘性能好 ④不耐热
⑤耐化学腐蚀
A.①②③ B.①③⑤
C.①②③④⑤ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是( )
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.将足量CuSO4溶解在0.1 mol·L-1 H2S溶液中,Cu2+的最大浓度为1.3×10-35 mol·L-1
C.因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生
D.向H2S的饱和溶液中通入少量SO2气体,溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,M(OH)2(s)??M2+(aq)+2OH-(aq) Ksp=a。c(M2+)=b mol·L-1时,溶液的pH等于( )
A.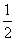 lg(
lg(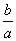 ) B.
) B.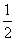 lg(
lg(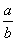 )
)
C.14+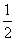 lg(
lg(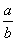 ) D.14+
) D.14+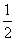 lg(
lg(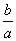 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验:①0.1 mol·L-1MgCl2溶液和0.2 mol·L-1NaOH溶液等体积混合得到浊液a,取少量浊液a过滤得到滤液b和白色沉淀c;②向浊液a中滴加0.1 mol·L-1FeCl3溶液,出现红褐色沉淀。下列分析不正确的是( )
A滤液b的pH=7
B.②中颜色变化说明Mg(OH)2转化为Fe(OH)3
C.实验可以证明Fe(OH)3的溶解度比Mg(OH)2的小
D.浊液a中存在沉淀溶解平衡:Mg(OH)2(s)??
Mg2+(aq)+2OH-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如下图所示。
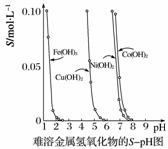
(1)pH=3时溶液中铜元素的主要存在形式是________(写化学式)。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为______(填字母)。
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,______(填“能”或“不能”)通过调节溶液pH的方法来除去,理由是______________________________________________。
(4)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的________除去它们(填字母)。
A.NaOH B.FeS C.Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的书写及对应的表述均正确的是:
A.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量。则Fe(s)+S(s)===FeS(s) ΔH=-95.6 kJ·mol-1
B.稀醋酸与0.1 mol·L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
C.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
D.已知2C(s)+O2(g)=2CO(g)ΔH=-221 kJ·mol-1,则C的燃烧热ΔH=-110.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
柑橘中柠檬烯的结构可表示为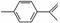 ,下列关于这种物质的说法中正确的是( )
,下列关于这种物质的说法中正确的是( )
A.与苯的结构相似,性质也相似
B.可使溴的四氯化碳溶液褪色
C.易发生取代反应,难发生加成反应
D.该物质极易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com