
分析 (1)能层序数相同时,能级越高,能量越高;能级符号相同时,能层序数越大,能量越高;在氮气分子中为氮氮叁键即1个σ键2个π键;一般情况下,主族序数=原子核外电子数(价电子数)=元素的最高化合价,但有例外如F、O,以此规律判断;
(2)某元素+3价离子基态时和氩原子的电子构型相同,该元素质子数=18+3=21;某元素+3价离子基态时的3d轨道半充满,则基态原子外围电子排布为3d64s2.
解答 解:(1)能级符号相同时,能层序数越大,能量越高,故ns<(n+1)s,在氮气分子中为氮氮叁键即1个σ键2个π键,所以σ键数<π键数,一般情况下,主族序数=原子核外电子数(价电子数)=元素的最高化合价,但有例外如F、O,
故答案为:<;<;=;=;
(2)某元素+3价离子基态时和氩原子的电子构型相同,该元素质子数=18+3=21,为Sc元素,离子符号为Sc3+;某元素+3价离子基态时的3d轨道半充满,则基态原子外围电子排布为3d64s2,为Fe元素,离子符号为Fe3+;
故答案为:Sc3+;Fe3+.
点评 本题考查能量变化、核外电子排布以及结构与性质、位置关系,难度不大,注意对核外电子排布规律的理解掌握等规律,熟知这些规律和特例是解题的基础,题目难度不大.


科目:高中化学 来源: 题型:解答题
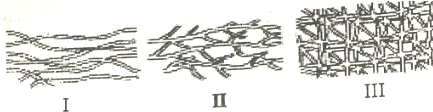
硫化橡胶 | 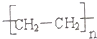 | 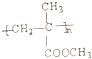 | |
| (1)结构形式示 意图 | |||
| (2)性质特点 | |||
| (3)主要应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6:3:2 | B. | 1:2:3 | C. | 1:1:1 | D. | 3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉加入三氯化铁溶液中:Fe+2Fe3+═3Fe2+ | |
| B. | 钠与水的反应Na+2H2O═Na++2OH -+H2↑ | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 大理石溶于醋酸的反应CaCO3+2H+═Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com