
在常温常压下,已知:
①4Fe(s)+3O2(g)===2Fe2O3(s) ΔH1
②4Al(s)+3O2(g)===2Al2O3(s) ΔH2
③2Al(s)+Fe2O3(s)===Al2O3(s)+2Fe(s) ΔH3
则ΔH3与ΔH1、ΔH2之间的关系正确的是( )
A.ΔH3=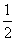 (ΔH1+ΔH2) B.ΔH3=ΔH2-ΔH1
(ΔH1+ΔH2) B.ΔH3=ΔH2-ΔH1
C.ΔH3=2(ΔH1+ΔH2) D.ΔH3=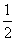 (ΔH2-ΔH1)
(ΔH2-ΔH1)
科目:高中化学 来源: 题型:
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O====CH3COOH+4H+。下列有关说法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为:CH3CH2OH+O2====CH3COOH+H2O
D.正极上发生的反应是:O2+4e-+2H2O====4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
pH相同的盐酸溶液与醋酸溶液分别和锌粒反应,若最后锌都已完全溶解,放出的气体一样多,下列说法正确的是( )
A.反应所需时间:醋酸>盐酸
B.整个反应阶段的平均反应速率:醋酸>盐酸
C.开始的反应速率:盐酸>醋酸
D.参加反应的锌的质量:盐酸=醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为14;X原子的内层电子数与Y原子的最外层电子数相等;X原子的核外电子总数与Z原子的最外层电子数相等。下列说法正确的是( )
A.X的氧化物都能与水反应生成酸
B.Y和Z组成的化合物是离子化合物
C.Z的离子半径比Y的离子半径小
D.X的气态氢化物分子与Z的离子具有相同的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1 mol某纯物质的热效应,单位常用kJ·mol-1表示。已知在25℃的条件下:
Ag2O(s)+2HCl(g)===2AgCl(s)+H2O(l) ΔH1=-324.4 kJ·mol-1
2Ag(s)+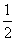 O2(g)===Ag2O(s) ΔH2=-30.56 kJ·mol-1
O2(g)===Ag2O(s) ΔH2=-30.56 kJ·mol-1
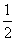 H2(g)+
H2(g)+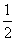 Cl2(g)===HCl(g) ΔH3=-92.21 kJ·mol-1
Cl2(g)===HCl(g) ΔH3=-92.21 kJ·mol-1
H2(g)+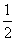 O2(g)===H2O(l) ΔH4=-285.6 kJ·mol-1
O2(g)===H2O(l) ΔH4=-285.6 kJ·mol-1
则25℃时氯化银的标准生成热为( )
A.-126.89 kJ·mol-1 B.-324.4 kJ·mol-1
C.-30.56 kJ·mol-1 D.题中数据不足,无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是人们开发利用的一种新能源,已知:
①2H2(g)+O2(g)===2H2O(l) ΔH1=-571.8 kJ·mol-1
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH2=-192.9 kJ·mol-1
③CH3OH(l)===CH3OH(g) ΔH3=+37.4 kJ·mol-1
(1)写出表示甲醇燃烧热的热化学方程式:__________________________________________________________
__________________________________________________________。
(2)H2的燃烧热为__________________________________________________________。
(3)二甲醚也是一种新型燃料,1 mol二甲醚蒸气完全燃烧生成CO2和液态水时放出1 455 kJ热量,若1 mol二甲醚和甲醇的混合气体完全燃烧生成CO2和液态水时共放出1 224.9 kJ热量,则混合气体中甲醇和二甲醚的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在体积为2 L的密闭容器中,充入1 mol 气体A和a mol气体B,发生如下反应:A(g)+B(g)2C(g)。5 min 后反应达到平衡时n(A)为0.4 mol。在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度的关系如图所示。下列叙述正确的是(双选)( )
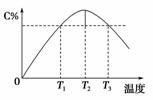
A.0~5 min,C物质的平均反应速率为0.12 mol·L-1·min-1
B.图中T1时正反应速率等于T3时正反应速率
C.该反应T2时的平衡常数大于T3时的平衡常数
D.图中T2时,若只增大压强,则正、逆反应速率不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
表中,对陈述Ⅰ、Ⅱ的正确性及两者之间是否具有因果关系判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 碳酸钠可用于治疗胃酸过多 | Na2CO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 将Na2O2投入水中充分反应后,滴入酚酞变红 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
| C | 金属钠具有强还原性 | 高压钠灯发生透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | 保存NaOH溶液的试剂瓶用橡皮塞 | NaOH能与玻璃中的SiO2发生反应 | Ⅰ对,Ⅱ对,有 |
|
| A. | A、 | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com