
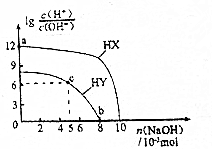
| A. | HX的酸性弱于HY | |
| B. | a点由水电离出的c(H+)=10-12mol•L-1 | |
| C. | c点溶液中:c(Y-)>c(HY) | |
| D. | b点时酸碱恰好完全中和 |
分析 A.lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$的值大;
B.a点lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$=12,则溶液中c(H+)=0.1mol/L;
C.c点lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$=6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY;
D.浓度均为0.1mol•L-1、体积均100mL的HY与NaOH恰好中和消耗NaOH为0.01mol.
解答 解:A.lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$的值大,所以HX的酸性大于HY,故A错误;
B.a点lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$=12,则溶液中c(H+)=0.1mol/L,溶液中水电离的c(H+)=$\frac{1{0}^{-14}}{0.1}$=10-13mol•L-1,故B错误;
C.c点lg$\frac{c{(H}^{+})}{c{(OH}^{-})}$=6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,由于溶液显酸性,所以HY的电离程度大于NaY的水解程度,所以c(Y-)>c(HY),故C正确;
D.浓度均为0.1mol•L-1、体积均100mL的HY与NaOH恰好中和消耗NaOH为0.01mol,而b点时消耗的NaOH为0.008mol,所以酸过量,故D错误.
故选C.
点评 本题考查酸碱混合溶液酸碱性判断及溶液中离子浓度大小比较,涉及盐类的水解和弱酸的电离等,题目难度中等,侧重于考查学生的分析能力和计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 用活性炭为蔗糖脱色和用臭氧漂白纸浆原理相似 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 奥运会中采用的新型氢动力计程车可以降低PM2.5的排放,减小大气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某品牌化妆品声称“我们拒绝化学,本品不含任何化学物质” | |
| B. | 用漂粉精和洁厕灵的混合液清洗马桶效果更佳 | |
| C. | 最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物 | |
| D. | 新核素的发现意味着新元素的合成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质溶液质童增加6.4g | B. | 阴极质量增加6.4g | ||
| C. | 阴极增加的质量小于6.4g | D. | 溶液中Cu2+浓度完全保持不变. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL1mol/L的Na3PO4溶液中含有离子数多于0.4NA | |
| B. | 1molAlCl3跟水反应完全转化成氢氧化铝胶体后,生成胶体粒子的数目为1NA | |
| C. | 12g石墨晶体中含有碳碳键数目为2×6.02×1023 | |
| D. | 标准状况下,22.4LCHCl3中含有氯原子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验是进行化学研究的重要手段之一.请回答下列问题:
实验是进行化学研究的重要手段之一.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com