
| A. | 1.0L1.0mol•L-1CH3COOH溶液中,CH3COOH分子数为NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为10 NA | |
| C. | 标准状况下,22.4L甲醇完全燃烧后生成的CO2分子数目约为NA | |
| D. | 2.8 g乙烯和丁烯的混合气体中所含碳原子数为0.2NA |
分析 A.醋酸为弱电解质,部分电离;
B.1个甲基含有9个电子;
C.气体摩尔体积使用对象为气体;
D.结合乙烯和丁烯最简式相同为CH2,只需计算2.8gCH2中含的碳原子数.
解答 解:A.醋酸为弱电解质,部分电离,所以1.0L1.0mol•L-1CH3COOH溶液中,CH3COOH分子数小于NA,故A错误;
B.1 mol甲基(-CH3)所含的电子总数为9NA,故B错误;
C.气体摩尔体积使用对象为气体,标况下甲醇为液体,不能使用气体摩尔体积,故C错误;
D.乙烯和丁烯最简式相同为CH2,2.8gCH2中含的碳原子数=$\frac{2.8g}{14g/mol}$×NA=0.2NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,质量换算物质的量计算微粒数,化学键数的方法与判断,题目难度中等,熟练掌握公式的使用和物质的结构是解题关键.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:选择题
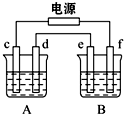 如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中d极产生具有氧化性的气体,在标准状况下为2.24L.下列说法正确的是( )
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中d极产生具有氧化性的气体,在标准状况下为2.24L.下列说法正确的是( )| A. | 一段时间后A池溶液pH升高,B池中c(Cu2+)减小 | |
| B. | d、e两极都发生氧化反应 | |
| C. | e极应为粗铜板材料 | |
| D. | B池中f极质量减小12.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其单质在常温下与水反应不如钙剧烈 | |
| B. | 其碳酸盐难溶于水 | |
| C. | 其主要化合价为+1价 | |
| D. | 其氢氧化物不能使Al(OH)3溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与W形成的化合物均与BaCl2溶液反应产生沉淀 | |
| B. | Z、W的简单离子均可促进水的电离 | |
| C. | 原子半径:X<Y<Z<W | |
| D. | X与Y形成的化合物中均只含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某些花岗石产生氡(${\;}_{86}^{222}$Rn),从而对人体产生伤害,${\;}_{86}^{222}$Rn的质量数是222 | |
| B. | Se是人体必需的微量元素,${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同位素 | |
| C. | ${\;}_{6}^{13}$C-NMR(核磁共振)可用于含碳化合物的结构分析,${\;}_{6}^{13}$C的中子数为6 | |
| D. | 原子结构示意图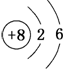 既可以表示16O,也可以表示18O 既可以表示16O,也可以表示18O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| B. | 在Cl2制备实验中,用饱和食盐水除去Cl2中的HCl气体,用NaOH溶液吸收尾气 | |
| C. | 除去CO2气体中混有的少量HCl,可以将气体通入饱和NaHCO3溶液中 | |
| D. | H2在Cl2中燃烧火焰呈淡蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
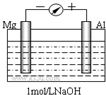 实验是化学的最高法庭.以镁条、铝片为电极,以稀NaOH溶液为电解质溶液构成的原电池,人们普遍认为铝是负极.某研究性学习小组为探究该原电池究竟谁是负极,发生怎样的电极反应,进行了如下实验:
实验是化学的最高法庭.以镁条、铝片为电极,以稀NaOH溶液为电解质溶液构成的原电池,人们普遍认为铝是负极.某研究性学习小组为探究该原电池究竟谁是负极,发生怎样的电极反应,进行了如下实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com