
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.分析 Ⅰ、(1)依据浓硫酸具有吸水性分析判断;
(2)依据浓硫酸具有脱水性分析;
(3)浓硫酸和铜反应生成硫酸铜、二氧化硫和水,依据浓硫酸的强氧化性和酸性分析;
Ⅱ.(1)根据实验步骤确定操作所需仪器;
(2)浓硫酸的物质的量浓度为c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$=18.4mol/L,结合溶液稀释前后溶质的物质的量不变计算;
(3)根据c=$\frac{n}{V}$结合操作的方法判断误差.
解答 解:Ⅰ、(1)浓硫酸可以干燥氢气,利用的是浓硫酸具有吸水性做干燥剂;
故答案为:B;
(2)浓硫酸使木条变黑是利用浓硫酸具有脱水性;
故答案为:C;
(3)热的浓硫酸与铜片反应生成硫酸铜、二氧化硫和水,表现了浓硫酸的酸性和强氧化性;
故答案为:AD;
Ⅱ.(1)配制100mL 1mol/L的稀硫酸,可用量筒量取一定体积的浓硫酸,在烧杯中加水稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,并洗涤烧杯,将洗涤液一并转移到容量瓶中,加入蒸馏水至刻度线2~3cm时,改用教头滴管定容,则还需要的仪器有玻璃棒和100mL容量瓶,
故答案为:⑦⑧;
(2)浓硫酸的物质的量浓度为c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$=18.4mol/L,设需浓硫酸的体积为V,则有V×18.4mol/L=0.1L×1mol/L,
V=0.0054L=5.4mL,
故答案为:5.4;
(3)A.量取浓H2SO4时,俯视刻度线,会导致量取液体体积偏小,浓度偏低,故A错误;
B.定容时,俯视容量瓶刻度线,会导致体积偏小,浓度偏大,故B正确
C.配制前,容量瓶中有水珠,对实验没有影响,故C错误;
D.定容后摇匀发现液面下降而未向其中再加水,浓度没有影响,故D错误.
故答案为:B.
点评 本题考查较为综合,涉及浓硫酸的性质以及溶液的配制,侧重于学生的分析能力和实验能力的考查,难度不大,注意相关基础知识的积累.


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:解答题
 甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量铜粉除去Cu(NO3)2溶液中的Fe(NO3)3杂质 | |
| B. | 在物质提纯操作中不能用乙醇从碘水中萃取碘 | |
| C. | 向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | |
| D. | 向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
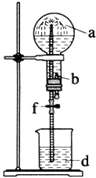 在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.a和b分别是( )
在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.a和b分别是( )| a(干燥气体) | b(液体) | |
| A | NO2 | 水 |
| B | CO2 | 水 |
| C | Cl2 | 饱和食盐水 |
| D | NH3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+和Fe2+ | B. | H+和Cu2+ | C. | Fe2+和Mg2+ | D. | Fe3+和Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCO2的质量为44g/mol | |
| B. | H2SO4的摩尔质量为98 | |
| C. | 标准状况下,气体摩尔体积约为22.4L | |
| D. | O2的相对分子质量为32 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
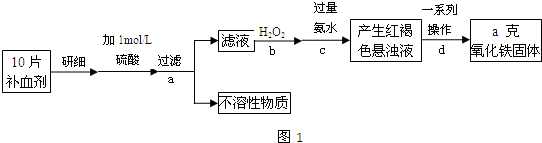
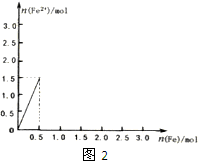
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在Cu催化作用下和O2反应时键①⑤断裂 | |
| B. | 和氢溴酸共热时键②断裂 | |
| C. | 和金属钠反应时键①断裂 | |
| D. | 和浓硫酸加热到170℃,键②⑤断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.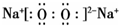 .
.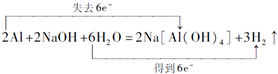 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com