
| A.NaOH | B.H2SO4 | C.Na2SO4 | D.CuSO4 |
科目:高中化学 来源:不详 题型:单选题
| A.35.5∶108 | B.16∶207 | C.8∶1 | D.108∶35.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
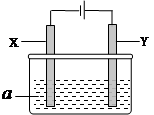
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 等杂质离子,下列加入顺序合理的是 ②。
等杂质离子,下列加入顺序合理的是 ②。| A.碳酸钠、氢氧化钠、氯化钡 | B.碳酸钠、氯化钡、氢氧化钠 |
| C.氢氧化钠、碳酸钠、氯化钡 | D.氯化钡、氢氧化钠、碳酸钠 |
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶于酸的物质 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.④⑤⑥ | C.①③④ | D.②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
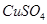 溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16。请回答:
溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16。请回答: 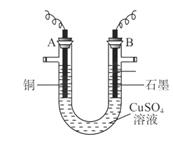
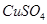 溶液)中,学习小组采用两套方案测定铜的相对原子质量。
溶液)中,学习小组采用两套方案测定铜的相对原子质量。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
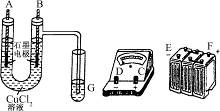
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.35.5∶108 | B.108∶35.5 |
| C.8∶1 | D.1∶2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
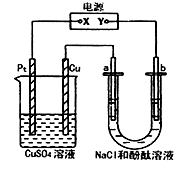
| A.x是正极,y是负极,CuSO4溶液的pH 逐渐减小 |
| B.x是正极,y是负极,CuSO4溶液的pH保持不变 |
| C.x是负极,y是正极,CuSO4溶液的pH 逐渐减小 |
| D.x是负极,y是正极,CuSO4溶液的pH保持不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com