
 Cu(s)ЃЋH2O(g)дкЯрЭЌЕФФГЮТЖШЯТЕФЦНКтГЃЪ§ЗжБ№ЮЊK1КЭK2ЃЌИУЮТЖШЯТЗДгІЂлЃКCO(g)ЃЋH2O(g)
Cu(s)ЃЋH2O(g)дкЯрЭЌЕФФГЮТЖШЯТЕФЦНКтГЃЪ§ЗжБ№ЮЊK1КЭK2ЃЌИУЮТЖШЯТЗДгІЂлЃКCO(g)ЃЋH2O(g)  CO2(g)ЃЋH2(g)ЕФЦНКтГЃЪ§ЮЊKЁЃдђЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
CO2(g)ЃЋH2(g)ЕФЦНКтГЃЪ§ЮЊKЁЃдђЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)AЃЎЗДгІЂйЕФЦНКтГЃЪ§K1ЃН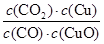 |
BЃЎЗДгІЂлЕФЦНКтГЃЪ§KЃН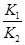 |
| CЃЎЖдгкЗДгІЂлЃЌКуШнЪБЃЌЮТЖШЩ§ИпЃЌH2ХЈЖШМѕаЁЃЌдђИУЗДгІЕФьЪБфЮЊе§жЕ |
| DЃЎЖдгкЗДгІЂлЃЌКуЮТКуШнЯТЃЌдіДѓбЙЧПЃЌH2ХЈЖШвЛЖЈМѕаЁ |
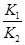 ЃЌBе§ШЗЁЃЗДгІЂлжаЃЌЮТЖШЩ§ИпЃЌH2ХЈЖШМѕаЁЃЌдђЦНКтЯђзѓвЦЖЏЃЌМДФцЗДгІЮЊЮќШШЗДгІЃЌе§ЗДгІЮЊЗХШШЗДгІЃЌгІЮЊІЄH<0ЃЌCДэЮѓЁЃЖдгкЗДгІЂлЃЌдкКуЮТКуШнЯТЃЌдіДѓбЙЧПЃЌШчГфШыЯЁгаЦјЬхЃЌдђЦНКтВЛвЦЖЏЃЌH2ЕФХЈЖШВЛБфЃЌDДэЮѓЁЃ
ЃЌBе§ШЗЁЃЗДгІЂлжаЃЌЮТЖШЩ§ИпЃЌH2ХЈЖШМѕаЁЃЌдђЦНКтЯђзѓвЦЖЏЃЌМДФцЗДгІЮЊЮќШШЗДгІЃЌе§ЗДгІЮЊЗХШШЗДгІЃЌгІЮЊІЄH<0ЃЌCДэЮѓЁЃЖдгкЗДгІЂлЃЌдкКуЮТКуШнЯТЃЌдіДѓбЙЧПЃЌШчГфШыЯЁгаЦјЬхЃЌдђЦНКтВЛвЦЖЏЃЌH2ЕФХЈЖШВЛБфЃЌDДэЮѓЁЃ


| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
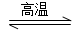 Si3N4(s)ЃЋ12HCl(g)ЁЁІЄH<0
Si3N4(s)ЃЋ12HCl(g)ЁЁІЄH<0ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
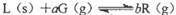 ДяЕНЦНКтЪБЃЌЮТЖШКЭбЙЧПЖдИУЗДгІЕФгАЯьШчЭМЫљЪОЃКЭМжабЙЧПP1>P2ЃЌxжсБэЪОЮТЖШЃЌyжсБэЪОЦНКтЛьКЯЦјжаGЕФЬхЛ§ЗжЪ§ЁЃОнДЫПЩХаЖЯ( )ЁЃ
ДяЕНЦНКтЪБЃЌЮТЖШКЭбЙЧПЖдИУЗДгІЕФгАЯьШчЭМЫљЪОЃКЭМжабЙЧПP1>P2ЃЌxжсБэЪОЮТЖШЃЌyжсБэЪОЦНКтЛьКЯЦјжаGЕФЬхЛ§ЗжЪ§ЁЃОнДЫПЩХаЖЯ( )ЁЃ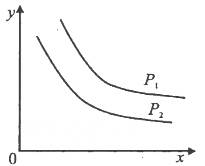
| AЃЎЩЯЪіЗДгІЪЧЗХШШЗДгІ | BЃЎЩЯЪіЗДгІЪЧЮќШШЗДгІ |
| CЃЎa>b | DЃЎa+1<b |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
 CO (g)+H2 (g)ЁЁІЄH="+131" kJЁЄmol-1
CO (g)+H2 (g)ЁЁІЄH="+131" kJЁЄmol-1| ШнЦї БрКХ | c(H2O) /molЁЄL-1 | c(CO) /molЁЄL-1 | c(H2) /molЁЄL-1 | vе§ЁЂvФцБШНЯ |
| Ђё | 0.06 | 0.60 | 0.10 | vе§=vФц |
| Ђђ | 0.06 | 0.50 | 0.40 | Ђй |
| Ђѓ | 0.12 | 0.40 | 0.80 | vе§<vФц |
| Ђє | 0.12 | 0.30 | Ђк | vе§=vФц |
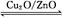 CH3OH(g)ЁЁІЄH>0,ИјКЯГЩМзДМЗДгІЬхЯЕжаЭЈШыЩйСПCOдђЦНКтЁЁЁЁЁЁЁЁвЦЖЏ,МѕаЁбЙЧПдђЦНКтЁЁЁЁЁЁЁЁвЦЖЏ,НЕЕЭЮТЖШдђЦНКтЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁвЦЖЏ(ЬюЁАЯђзѓЁБЁЂЁАЯђгвЁБЛђЁАВЛЁБ)ЁЃ
CH3OH(g)ЁЁІЄH>0,ИјКЯГЩМзДМЗДгІЬхЯЕжаЭЈШыЩйСПCOдђЦНКтЁЁЁЁЁЁЁЁвЦЖЏ,МѕаЁбЙЧПдђЦНКтЁЁЁЁЁЁЁЁвЦЖЏ,НЕЕЭЮТЖШдђЦНКтЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁвЦЖЏ(ЬюЁАЯђзѓЁБЁЂЁАЯђгвЁБЛђЁАВЛЁБ)ЁЃ ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
 C(g)ЃЋD(g) ІЄHЃМ0ЁЃЧыЛиД№ЯТСаЮЪЬт:
C(g)ЃЋD(g) ІЄHЃМ0ЁЃЧыЛиД№ЯТСаЮЪЬт:ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎKдНДѓЃЌЗДгІЮяЕФзЊЛЏТЪдНаЁ |
| BЃЎKгыЗДгІЮяЕФХЈЖШгаЙи |
| CЃЎKгыЩњГЩЮяЕФХЈЖШгаЙи |
| DЃЎKгыЮТЖШгаЙи |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
 pC(g)ДяЕНЦНКтЪБЃЌВтЕУc(A)ЮЊ0.5 molЁЄL-1ЃЛдкЮТЖШВЛБфЕФЬѕМўЯТЃЌНЋШнЦїЬхЛ§РЉДѓвЛБЖЃЌЕБДяЕНЦНКтЪБЃЌВтЕУc(A)ЮЊ0.3 molЁЄL-1ЁЃдђЯТСаХаЖЯе§ШЗЕФЪЧ( )
pC(g)ДяЕНЦНКтЪБЃЌВтЕУc(A)ЮЊ0.5 molЁЄL-1ЃЛдкЮТЖШВЛБфЕФЬѕМўЯТЃЌНЋШнЦїЬхЛ§РЉДѓвЛБЖЃЌЕБДяЕНЦНКтЪБЃЌВтЕУc(A)ЮЊ0.3 molЁЄL-1ЁЃдђЯТСаХаЖЯе§ШЗЕФЪЧ( )ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com