

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A���÷�Ӧ��N2O4����������ƫ�������ǻ�ԭ�� |
| B��N2���������CO2�ǻ�ԭ���� |
| C��CO2���������N2�ǻ�ԭ���� |
| D��ÿ��0.6molN2���ɣ�ת�Ƶ�����ĿΪ2.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
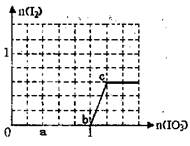
| A����Ӧ�����е����������ΪSO3 |
| B��a��ʱʣ��NaHSO3�����ʵ���Ϊ1.2 mol |
| C��b��ʱ�Ļ�ԭ���������KI��NaI |
| D������Һ��I-��I2�����ʵ���֮��Ϊ1��1ʱ�������KIO3Ϊ1.1 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��
�� bO2��Cr3����Ӧ��������Cr2O72����Pb2����������1mol C
bO2��Cr3����Ӧ��������Cr2O72����Pb2����������1mol C r2O72��
r2O72�� ____��
____���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
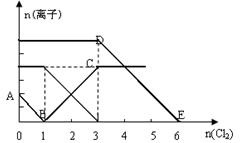
| A��B��ʱ��Һ�к���I-��Br- |
B��DE�α�ʾn (F e2+)���仯��� e2+)���仯��� |
| C��ԭ��Һ��n (Fe2+) ��n (I-) ��n (Br-) =" 3" ��1 ��2 |
| D����ͨ��2mol Cl2ʱ����Һ�з��������ӷ�Ӧ�ǣ�2Fe2+ + 2I- + 2Cl2 = 2Fe3+ + I2 + 4 Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com