
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结
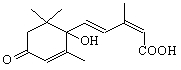 构如右图,下列关于该物质的说法正确的是
构如右图,下列关于该物质的说法正确的是
A.其分子式为C15H18O4
B.既能发生加聚反应,又能发生缩聚反应
C.分子中含有2个手性碳原子
D.既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色
 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
下列不能证明氯的非金属性比硫强的实验是( )
A.HCl比H2S稳定
B.HCl溶液(盐酸)的酸性比H2S溶液(氢硫酸)的酸性强
C.氯水滴入氢硫酸溶液中可出现淡黄色沉淀 D.氯气比硫有更强的氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
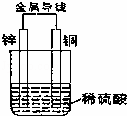
如图所示进行实验,下列说法正确的是( )
|
| A. | 铜片上冒气泡,该气体是H2,铜片是正极,该装置是原电池 |
|
| B. | 锌片质量减小,锌片是负极,发生还原反应 |
|
| C. | 电子流向:锌→导线→铜→稀硫酸→锌,形成一个闭合回路 |
|
| D. | 溶液中的阳离子移向负极,阴离子移向正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两容器中均进行反应:N2+3H2⇌2NH3,在相同时间内,甲容器中断裂1molN≡N键且同时形成3molH﹣H键,乙容器中断裂0.5molN≡N键且同时断裂3molN﹣H键,下列说法正确的是( )
|
| A. | 甲容器中的反应速率一定大于乙容器中的反应速率 |
|
| B. | 甲容器中的反应速率可能小于乙容器中的反应速率 |
|
| C. | 无法判断两容器中的上述反应是否都达到了平衡状态 |
|
| D. | 上述两容器中的反应一定是在相同温度和相同压强下进行的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下容积为10L的密闭容器中加入一定量的SO2、O2并发生如下反应:2SO2(g)+O2(g)⇌2SO3(g),经过10分钟测得容器中三种物质SO2、O2、SO3的物质的量分别为3mol、9mol、2mol,再经过t分钟时反应达到了平衡状态,且已知平衡状态时SO2的转化率为80%(提示:SO2的转化率是指反应掉的SO2占原来SO2总量的百分数),回答下列问题:
(1)前10分钟SO2的平均反应速率为 ,10分钟时该反应是否达到平衡状态
(填“是”、“否”、“不一定”),开始时加入容器中的O2的物质的量为 ;
(2)平衡状态时容器中O2的浓度为 ,关于t分钟的下列说法正确的是 ;
A.t肯定大于10
B.t肯定小于10
C.t一定等于10
D.t可能大于10、也可能等于或小于10
(3)改变温度化学平衡发生移动,最后重新达到新的平衡状态,在新平衡状态下测得各物质的浓度数据如下,其中合理的是 ;
A.c(SO2)=0.2mol/L,c(O2)=0.8mol/L,c(SO3)=0.3mol/L
B.c(SO2)=0.2mol/L,c(O2)=0.85mol/L,c(SO3)=0.3mol/L
C.c(SO2)=0.2mol/L,c(O2)=0.8mol/L,c(SO3)=0.4mol/L
D.c(SO2)=0.05mol/L,c(O2)=0.775mol/L,c(SO3)=0.35mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.实验室常见的几种气体发生装置如图A、B、C所示:
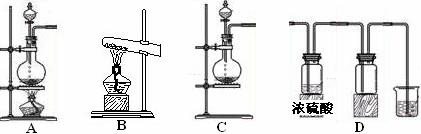
(1) 实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为
。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是
_____________(填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可以是下列气体中的________。
①CO2 ②NO ③Cl2 ④H2 ⑤HCl
其中在D装置中连接小烧杯的目的是 。
Ⅱ.某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
(4)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3 ,钴的化合价为________,制备X的化学方程式为
已知:X的化学式类似下列化学式
氢氧化二氨合银:Ag(NH3)2OH 、硫酸四氨合铜:Cu(NH3)4SO4
(5)氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。
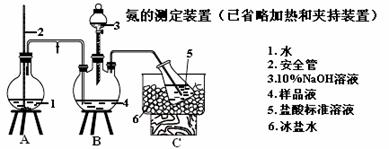
①盛放5(盐酸标准溶液)的仪器名称
②装置中安全管的作用原理是
③样品中氨的质量分数表达式为
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是( )
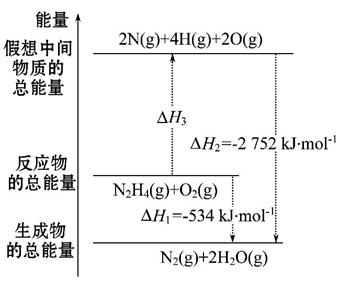
A.194 B.391 C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中进行反应:
2SO2(g)+O2(g)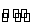 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达平衡时,可能存在的数据是( )
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达平衡时,可能存在的数据是( )
A.SO2为0.4 mol·L-1,O2为0.2 mol·L-1
B.SO2为0.25 mol·L-1
C.SO2、SO3均为0.15 mol·L-1
D.SO3为0.4 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com