
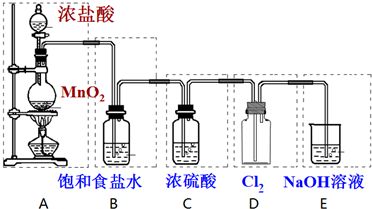
分析 (1)依据反应中是否有化合价变化判断;
(2)浓盐酸具有挥发性,制取的氯气中混有杂质氯化氢,需要用饱和食盐水除去;
(3)依据氯气密度大于空气密度结合D中长进短出特点解答;
(4)氯气有毒,直接排放能够引起空气污染,氯气能够与氢氧化钠溶液反应,被氢氧化钠吸收;
(5)计算标准状况下4.48L的Cl2的物质的量,依据方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O计算需要二氧化锰的质量;
(6)根据氯气与水反应生成的次氯酸见光易分解角度分析.
解答 解:(1)制取氯气的方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应中氯元素、锰元素化合价发生变化,属于氧化还原反应;
故答案为:是;
(2)制取的氯气中混有氯化氢气体,由于氯气在饱和食盐水中的溶解度较小,则可以用饱和食盐水除去氯气中的氯化氢杂质,
故答案为:除去氯气中的氯化氢;
(3)氯气密度大于空气密度,且D中导气管为长进短出,所以是向上排气法收集;
故答案为:向上排气法;
(4)氯气有毒,直接排放能够引起空气污染,氯气能够与氢氧化钠溶液反应,被氢氧化钠吸收,通常用氢氧化钠溶液吸收过量的氯气;
故答案为:吸收过量的氯气,进行尾气处理;
(5)算标准状况下4.48L的Cl2的物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,设需要二氧化锰的质量为m,则:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
87 1
m 0.2mol 解得m=17.4g;
故答案为;17.4;
(6)如果要用氯气消毒过的自来水来养金鱼,由于次氯酸见光易分解,可将自来水放在阳光下暴晒,或用强光照射自来水,也可以用紫外线照射自来水,将次氯酸除去,
故答案为:将自来水放在阳光下暴晒(或用强光照射自来水或用紫外线照射自来水).
点评 本题考查了氯气的制备、提纯和收集,熟悉制备原理,明确氯气的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 硅酸、氯化铁溶液均为胶体 | B. | 水玻璃、明矾溶液均为混合物 | ||
| C. | 硫酸、纯碱、NaCl分别属于酸、碱、盐 | D. | KCl和Cu均属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某蓝色溶液中加NaOH溶液,生成蓝色沉淀,说明原溶液中有Cu2+ | |
| B. | 某溶液中加BaCl2溶液,生成白色沉淀,继续滴加稀硝酸沉淀不溶解,说明原溶液中有SO42- | |
| C. | 某溶液中加硝酸银溶液,生成白色沉淀,继续滴加稀硝酸有部分沉淀不溶解,说明原溶液中一定有Cl- | |
| D. | 某溶液中加稀硫酸溶液生成无色无味气体,该气体能使澄清石灰水变浑浊,说明原溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
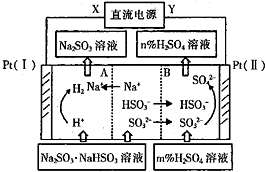
| A. | Pt(Ⅱ)为阳极 | B. | 阳极区[H+]增大 | ||
| C. | 图中的n<m | D. | 阴极电极反应式为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 10HCl□
10HCl□查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑧ | B. | ②③④⑤⑥⑦ | C. | ③⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+l、+2 等,故能形成多种铜的化合物.
铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+l、+2 等,故能形成多种铜的化合物. 查看答案和解析>>
科目:高中化学 来源: 题型:解答题
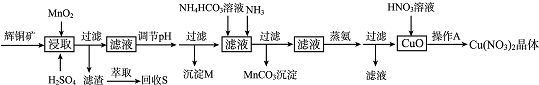
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com