
| A. | 升温 | B. | 及时分离出氨气 | C. | 加入催化剂 | D. | 增大容器内压强 |
分析 依据影响化学反应速率的因素分析,增大压强,浓度、升高温度速率都增大,平衡是气体体积减小的放热反应,依据平衡移动原理分析判断.
解答 解:A、反应是放热反应,升温,正逆反应速率都增大,平衡逆向进行,故A错误;
B、分离出氨气,降低氨气浓度,正反应速率不变,逆反应速率减小,平衡移动后速率都减小,平衡正向进行,故B错误;
C、加入催化剂,正逆反应速率均同等程度增大,平衡不移动,故C错误;
D、增大压强,正逆反应速率都增大,平衡向气体体积减小的方向进行,即平衡正向移动,故D正确;
故选D.
点评 本题考查了化学平衡移动原理的分析应用,反应特征和压强改变对反应速率的影响分析是解题关键,题目较简单.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| B. | 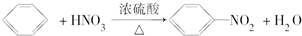 | |
| C. | CH3CH2OH+CH3COOH$→_{△}^{催化剂}$CH3COOC2H5+H2O | |
| D. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数:Y>X>W>Z | B. | 原子半径:Z>W>X>Y | ||
| C. | 电负性:Y>X>W>Z | D. | 简单气态氢化物的沸点:Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个反应都是置换反应 | |
| B. | 反应②是放热反应 | |
| C. | 两个反应都有化学能与热能之间的转化 | |
| D. | 两个反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
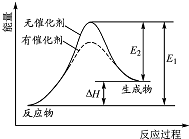 某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A. | 催化剂能改变该反应的焓变 | B. | 催化剂能降低该反应的活化能 | ||
| C. | 该反应为放热反应 | D. | E1 越大,表明该反应越容易发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将0.2 mol•L-1 NaA溶液和0.1 mol•L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)═c(A-)+c(Cl-) | |
| B. | 在25℃100 mL NH4Cl溶液中:c(Cl-)═c(NH4+)+c(NH3•H2O) | |
| C. | 0.1 mol•L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 0.1 mol•L-1的NaHCO3溶液中:c(Na+)═c(HCO3-)+c(H2CO3)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2的摩尔质量为71g/mol | |
| B. | 1mol Na2O2与H2O完全反应转移的电子数为NA | |
| C. | 32 g O2气体所含原子数为2NA | |
| D. | 常温常压下,11.2 L氯气含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com