
| A�� | ��ʱ��ȥ������̼������Ӧ���ʼӿ� | |
| B�� | �����������䣬�����������H��� | |
| C�� | ����ѹǿ������Ӧ���������淴Ӧ���ʼ�С | |
| D�� | �����¶ȣ�����߷�Ӧ���ת���� |
���� �÷�Ӧ������Ӧ���������С�ķ��ȷ�Ӧ������������ĸı�Է�Ӧ���ʺ�ƽ���ƶ���Ӱ�����������������䣬���������ܶ�ʼ�ղ��䣮
��� �⣺A����ȥ������̼������Ũ�Ƚ��ͣ�����Ӧ������������A����
B��������Ӱ��ƽ���ƶ������ԣ����������H���䣬��B����
C����Ӧǰ�����������С������ѹǿƽ��������У���Ӧ�����������淴Ӧ���ʶ���������Ӧ��������Ĵ�C����
D������ƽ�������ƶ�����Ӧ��ת��������D��ȷ��
��ѡD��
���� ���⿼���˴�����ƽ���ƶ���Ӱ�졢Ӱ�췴Ӧ���ʵ����ء���ѧƽ��״̬���жϣ���Ŀ�Ѷ��еȣ�


 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶��ϵ�һ���¿���ѧ���������棩 ���ͣ�ѡ����
�����Ϊ2L�������м���1mol N2��6mol H2���ϳɰ���2����֮��ﵽƽ�⣬��õ���Ϊ0.6mol ���������ķ�Ӧ�����ǣ� ��
���������ķ�Ӧ�����ǣ� ��
A��0.1mol/��L•s�� B��0.2mol/��L•s�� C��0.3mol/��L•s�� D��0.6mol/��L•s��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
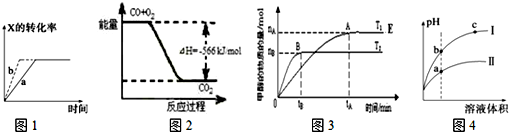
| A�� | ͼ1��ʾ����Ӧ��X��g��+2Y��g��?3Z��g����b��ѹǿһ����a�� | |
| B�� | ͼ2��ʾCO����CO2�ķ�Ӧ���̺�������ϵ | |
| C�� | ͼ3��ʾ��ӦCO+2H2?CH3OH��g���������¶�T2��T1���������������������£�������E�����ϵ�����ѹ����ԭ����$\frac{1}{2}$��ƽ�������ƶ�������Ũ������ | |
| D�� | ͼ4��ʾ����ˮϡ��pH��ͬ������ʹ��ᣬ���ʾ���ᣬ���ʾ���ᣬ����Һ�����ԣ�c��b��a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���º��ݣ�����N02���壬��ת�������� | |
| B�� | ��ѹ��ƽ�����淴Ӧ�����ƶ������������ɫ���� | |
| C�� | ��ƽ�ⳣ��������������������¶Ȼ��С����ϵ��ѹǿ | |
| D�� | ��2v����NO��=v����O2��ʱ����Ӧ�ﵽ��ѧƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͭ�Ľ�����Ա���������ͭ�������κ�ǿ�ᷢ����Ӧ | |
| B�� | Ũ������������������Ϊ�����ǿ������ | |
| C�� | ����Al2O3�����������������������ռ� | |
| D�� | ��ˮ��Ͳ�������ʯ��ʯ��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
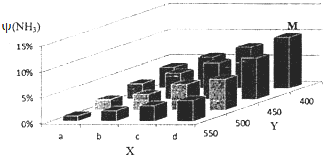 �ϳɰ��Ĺ�ҵ�������������������ʳ���⣬���ش�Ļ�ѧ�о��ɹ����ֽ�lmolN2��3molH2Ͷ��1L���ܱ���������һ�������£�����N2��g��+3H2��g��?2NH3��g����H��0��Ӧģ������ϳɰ��Ĺ�ҵ�����������ı�ijһ����������¶Ȼ�ѹǿ��ʱ��NH3����������ף�NH3���仯������ͼ��ʾ��
�ϳɰ��Ĺ�ҵ�������������������ʳ���⣬���ش�Ļ�ѧ�о��ɹ����ֽ�lmolN2��3molH2Ͷ��1L���ܱ���������һ�������£�����N2��g��+3H2��g��?2NH3��g����H��0��Ӧģ������ϳɰ��Ĺ�ҵ�����������ı�ijһ����������¶Ȼ�ѹǿ��ʱ��NH3����������ף�NH3���仯������ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com