
| 浓硫酸 |
| 加热 |

 ,
, ;
;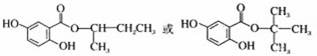 ,故答案为:
,故答案为: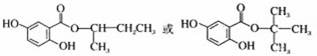 .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 实验目的 | 实验步骤及现象 | |||||||||
| A | 检验亚硫酸钠试样是否变质 | 试样
| ||||||||
| B | 检验某卤代烃是否是氯代烃 | 试样
| ||||||||
| C | 证明酸性条件下H2O2氧化性比I2强 | Nal溶液
| ||||||||
| D | 除去氯化钠晶体中少量硝酸钾 | 试样
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 的结构单元.B分子比A分子多了
的结构单元.B分子比A分子多了查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色).
如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成1mol Na2Mn5O10转移2mol电子 |
| B、AgCl是还原产物 |
| C、Na+不断向“水”电池的负极移动 |
| D、正极反应式:Ag+Cl--e-=AgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,将0.1mol?L-1盐酸滴入20mL 0.1mol?L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.
室温下,将0.1mol?L-1盐酸滴入20mL 0.1mol?L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com