
【题目】某学生称取9 g淀粉溶于水,测定淀粉水解的百分率,其过程如下(已知含有醛基的有机物可在碱性条件下与银氨溶液发生银镜反应生成单质Ag):
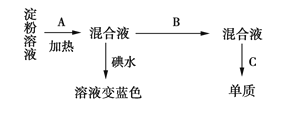
(1)填写各步所加试剂的名称:A.________;B.________;C._________。
(2)只加A而不加B是否可行?____(填“是”或“否”),理由是__________________________________。
(3)当析出2.16 g金属单质时,淀粉的水解率为___(已知1 mol醛基发生银镜反应时生成2 mol Ag)。
【答案】稀硫酸 氢氧化钠溶液 银氨溶液 否 用银氨溶液检验葡萄糖时必须在碱性条件下进行 18%
【解析】
(1)淀粉水解时用稀硫酸作催化剂,因此试剂A是稀硫酸。为检验水解产物葡萄糖,应先加入NaOH溶液中和稀硫酸,则试剂B是氢氧化钠溶液。葡萄糖与银氨溶液反应生成银单质,所以试剂C是银氨溶液。
(2)由于用银氨溶液检验葡萄糖时必须在碱性条件下进行,而淀粉水解需要用稀硫酸作催化剂,则只加A而不加B是不可行的。
(3)2.16g金属银的物质的量是![]() =0.02mol,由于1mol醛基发生银镜反应时生成2molAg,所以消耗葡萄糖的物质的量是0.01mol,则由(C6H10O5)n+nH2O
=0.02mol,由于1mol醛基发生银镜反应时生成2molAg,所以消耗葡萄糖的物质的量是0.01mol,则由(C6H10O5)n+nH2O![]() nC6H12O6可知,淀粉的水解率为
nC6H12O6可知,淀粉的水解率为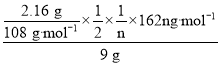
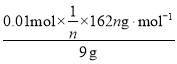 ×100%=18%。
×100%=18%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
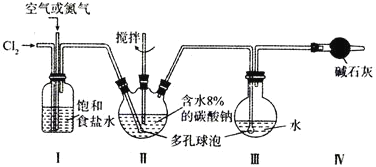
【题目】某实验室用下图所示装置制备高浓度的次氯酸,先在Ⅱ中生成![]() ,再在Ⅲ中得到HClO溶液。
,再在Ⅲ中得到HClO溶液。
已知:![]() 的沸点为
的沸点为![]() ,
,![]() 以上分解为
以上分解为![]() 和
和![]() ;
;![]() 极易溶于水并与水反应生成HClO。
极易溶于水并与水反应生成HClO。
(1)反应中通入空气或氮气的作用是________________,实验中控制氯气与空气或氮气的体积比的方法是_________。
(2)装置Ⅱ、Ⅲ中使用多孔球泡的作用是_________;装置Ⅱ中发生反应的化学方程式为_________。
(3)反应时,Ⅱ中要加装冷却装置,其原因是__________。
(4)已知次氯酸可被![]() 还原成
还原成![]() ,可利用此原理测定Ⅲ中所得次氯酸溶液的物质的量浓度。
,可利用此原理测定Ⅲ中所得次氯酸溶液的物质的量浓度。
![]() 此反应的化学方程式为__________________________。
此反应的化学方程式为__________________________。
![]() 量取
量取![]() 次氯酸溶液于烧杯中,加入足量的
次氯酸溶液于烧杯中,加入足量的![]() 溶液,混合均匀后再加入足量的
溶液,混合均匀后再加入足量的![]() 溶液,反应完全后过滤,洗涤,干燥,用电子天平称量,得到固体
溶液,反应完全后过滤,洗涤,干燥,用电子天平称量,得到固体![]() ,则所制取次氯酸的浓度为______
,则所制取次氯酸的浓度为______![]() 。
。
(5)若制得上述次氯酸溶液![]() ,转化过程中氯的损耗为
,转化过程中氯的损耗为![]() ,则至少需要标况下
,则至少需要标况下![]() __________L。
__________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl是生产印刷颜料酞菁蓝的重要原料,工业上可用一种低品位铜矿(主要成分CuS、Cu2S、CuO、Fe2O3、FeO及其他非酸溶性杂质)和软锰矿(主要成分为MnO2和其他非酸溶性杂质)来进行生产,过程如下:

回答下列问题:
(1)步骤Ⅰ中反应较多,下列反应是其中之一:Cu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+4H2O+S,该反应的氧化产物为____________________(填化学式)。
(2)为确定滤液1中是否含有Fe2+,首先用有机萃取剂除去溶液中MnSO4,再取下层水溶液进行检测,所用试剂为_____________________。
(3)步骤Ⅱ加入氨水控制溶液的pH为5左右,目的是______________________。
(4)为模拟步骤Ⅲ的生产过程,某同学设计如下实验,下列有关叙述正确的是_____________。

A.a通入CO2,然后b通入NH3;c中放碱石灰
B.b通入NH3,然后a通入CO2;c中放碱石灰
C.a通入NH3,然后b通入CO2;c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3;c中放蘸稀硫酸|的脱脂棉
(5)步骤Ⅳ的滤液中主要成分X是步骤Ⅱ和步骤Ⅲ都有的产物,可以回收作为肥料使用,该肥料_______(填“可以”或“不可以”)与草木灰(有效成分K2CO3)共用,简述原因:__________。
(6)已知CuCl为难溶于水的白色沉淀,写出步骤Ⅴ发生反应的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某红色固体粉末样品可能含有![]() 和
和![]() 中的一种或两种,某化学兴趣小组对其组成进行探究.资料支持:
中的一种或两种,某化学兴趣小组对其组成进行探究.资料支持:![]() 在酸性溶液中会发生反应:
在酸性溶液中会发生反应:![]()
方案一:
(1)学生甲取少量样品于烧杯中,加入过量浓硝酸,产生一种红棕色的气体.由此可得出样品中一定含有____,写出产生上述气体的化学方程式___。
(2)进一步探究样品中另一种成分.实验操作步骤为:取少量上述溶液,___。
方案二:
(3)学生乙取少量样品于烧杯中,加入过量稀硫酸,并作出如下假设和判断,结论正确的是______。
A.若固体全部溶解,说明样品一定含有![]() ,一定不含有
,一定不含有![]()
B.若固体部分溶解,说明样品一定含有![]() ,一定不含有
,一定不含有![]()
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,说明样品一定含有![]() 和
和![]()
方案三:学生丙利用如图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成.回答下列问题:
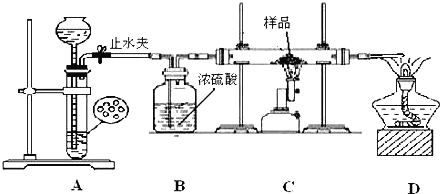
(4)装置A是氢气的发生装置,可以使用的药品是______。
A.氢氧化钠溶液和铝片 B.稀硝酸和铁片 C.稀硫酸和锌片 D.浓硫酸和镁片
(5)下列实验步骤的先后顺序是______(填序号)。
①打开止水夹; ②关闭止水夹; ③点燃C处的酒精喷灯;④熄灭C处的酒精喷灯 ⑤收集氢气并验纯
(6)假设样品全部参加反应,若实验前样品的质量为1.6克,实验后称得装置C中固体的质量为1.3克.则样品的组成是______。(可能用到的相对原子质量:Fe:56Cu:64C:12O:16 )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质和化合物在工农业生产中有着重要的应用,而![]() 直接排放会对环境造成危害。
直接排放会对环境造成危害。
I.已知:重晶石![]() 高温缎烧可发生一系列反应,其中部分反应如下:
高温缎烧可发生一系列反应,其中部分反应如下:
![]()
![]()
![]()
![]()
已知:![]()
![]()
则:![]()
![]() _____________;
_____________;
![]() 的尾气处理通常有以下几种方法:
的尾气处理通常有以下几种方法:
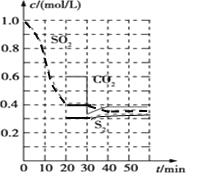
(1)活性炭还原法 反应原理:恒温恒容时![]() 反应进行到不同时间测得各物质的浓度如上图:
反应进行到不同时间测得各物质的浓度如上图:
![]() 反应速率表示为
反应速率表示为![]() _________________;
_________________;
![]() 时,改变某一条件平衡发生移动,则改变的条件最有可能是________________________;
时,改变某一条件平衡发生移动,则改变的条件最有可能是________________________;
![]() 时,平衡常数
时,平衡常数![]() _____________。
_____________。
(2)亚硫酸钠吸收法
![]() 溶液吸收
溶液吸收![]() 的离子方程式为____________
的离子方程式为____________
![]() 常温下,当吸收至
常温下,当吸收至![]() 时,吸收液中相关离子浓度关系一定正确的是_______
时,吸收液中相关离子浓度关系一定正确的是_______![]() 填序号
填序号![]()
![]()
![]()
![]()
![]() 水电离出
水电离出![]()
(3)电化学处理法
![]() 如下图所示,
如下图所示,![]() Ⅰ
Ⅰ![]() 电极的反应式为___________________;
电极的反应式为___________________;
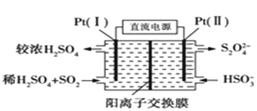
![]() 当电路中转移
当电路中转移![]() 时
时![]() 较浓
较浓![]() 尚未排出
尚未排出![]() ,交换膜左侧溶液中增加_______mol离子.
,交换膜左侧溶液中增加_______mol离子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出以乙炔为原料制备![]() (聚氯乙烯)的过程中所发生的反应类型:____________、_____________。
(聚氯乙烯)的过程中所发生的反应类型:____________、_____________。![]() (聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别
(聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别![]() 和
和![]() 有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:
有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:![]() 的单体和
的单体和![]() 的单体在足量空气中燃烧的实验现象的明显区别是__________。
的单体在足量空气中燃烧的实验现象的明显区别是__________。
(2)![]() (
(![]() )是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成
)是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成![]() 的单体的同分异构体的结构简式_________。
的单体的同分异构体的结构简式_________。
(3) “白色污染”是指各种塑料制品对环境的污染。焚烧塑料会生成有毒物质二噁英,二噁英是含有如图所示母体的系列化合物,下列关于如图所示物质的说法不正确的是___________________(填序号)。

a.该物质在氧气中完全燃烧的产物是![]() 和
和![]()
b.该物质属于烃
c.该物质的一卤代物只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知正四面体形分子E与线形分子G反应,生成四面体形分子L和直线形分子M。组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素。反应过程示意图如下,则下列判断中正确的是( )。
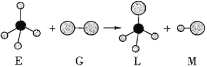
A.常温常压下,E是一种液态有机物B.M是一种含有非极性键的分子
C.干燥的G能漂白湿润的有色物质D.上述反应的类型是加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸、再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为
A. 0.1mol B. 0.2mol
C. 大于或等于0.2mo1,小于0.3mol D. 大于0.1mol,小于0.3mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com