
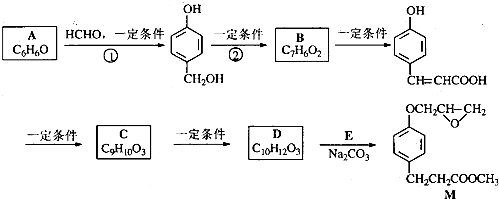
 、
、 .
. 分子式相同,且能使氯化铁溶液显紫色的同分异构体还有11种(不考虑立体异构),其中核磁共振氢谱为4组峰,且峰的面积比为2:2:1:3的结构简式(写出其中任意两种)是
分子式相同,且能使氯化铁溶液显紫色的同分异构体还有11种(不考虑立体异构),其中核磁共振氢谱为4组峰,且峰的面积比为2:2:1:3的结构简式(写出其中任意两种)是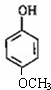 、
、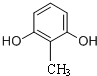 、
、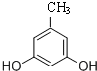 任意2种.
任意2种. 分析 A与甲醛反应生成 ,结合A的分子式可知A为
,结合A的分子式可知A为 ,反应①是苯酚与HCHO发生加成反应.结合B的分子式、B反应产物结构可知,反应②为醇的氧化反应,则B为
,反应①是苯酚与HCHO发生加成反应.结合B的分子式、B反应产物结构可知,反应②为醇的氧化反应,则B为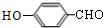 ,结合反应①可知
,结合反应①可知 与乙醛发生加成反应,再发生消去反应得到
与乙醛发生加成反应,再发生消去反应得到 ,结合M的结构简式与C的分子式,可知
,结合M的结构简式与C的分子式,可知 中碳碳双键与氢气发生加成反应生成C为
中碳碳双键与氢气发生加成反应生成C为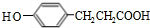 ,结合M的结构简式与D的分子式可知,C与甲醇发生酯化反应生成D为
,结合M的结构简式与D的分子式可知,C与甲醇发生酯化反应生成D为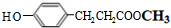 ,由M的结构可知E为
,由M的结构可知E为 ,据此解答.
,据此解答.
解答 解:A与甲醛反应生成 ,结合A的分子式可知A为
,结合A的分子式可知A为 ,反应①是苯酚与HCHO发生加成反应.结合B的分子式、B反应产物结构可知,反应②为醇的氧化反应,则B为
,反应①是苯酚与HCHO发生加成反应.结合B的分子式、B反应产物结构可知,反应②为醇的氧化反应,则B为 ,结合反应①可知
,结合反应①可知 与乙醛发生加成反应,再发生消去反应得到
与乙醛发生加成反应,再发生消去反应得到 ,结合M的结构简式与C的分子式,可知
,结合M的结构简式与C的分子式,可知 中碳碳双键与氢气发生加成反应生成C为
中碳碳双键与氢气发生加成反应生成C为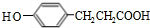 ,结合M的结构简式与D的分子式可知,C与甲醇发生酯化反应生成D为
,结合M的结构简式与D的分子式可知,C与甲醇发生酯化反应生成D为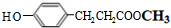 ,由M的结构可知E为
,由M的结构可知E为 .
.
(1)化合物M的化学式为C13H16O4,1mol化合物M完全燃烧消耗氧气为(13+$\frac{16}{4}$-$\frac{4}{2}$)mol=15mol,
故答案为:C13H16O4;15;
(2)由上述分析,可知反应①为加成反应,
故答案为:加成反应;
(3)A的结构简式为 ,E的结构简式为
,E的结构简式为 ,
,
故答案为: ;
; ;
;
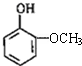
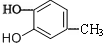
(4)与  分子式相同,且能使氯化铁溶液显紫色,说明含有酚羟基,同分异构体有
分子式相同,且能使氯化铁溶液显紫色,说明含有酚羟基,同分异构体有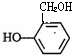 、
、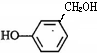 、
、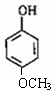 、
、 、
、 、
、 、
、 、
、 、
、 、
、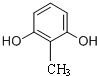 、
、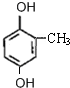 共11种,其中核磁共振氢谱为4组峰,且峰的面积比为2:2:1:3的结构简式有
共11种,其中核磁共振氢谱为4组峰,且峰的面积比为2:2:1:3的结构简式有 或
或 或
或 ,
,
故答案为:11; 、
、 、
、 任意2种.
任意2种.
点评 本题考查有机物的推断与合成,充分利用有机物的结构进行分析解答,注意碳链骨架、官能团的变化,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
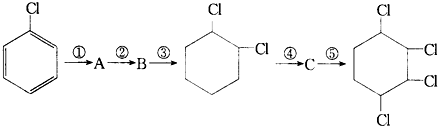
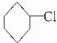 B
B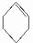
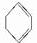 .
.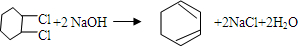 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl>NH3>HI | B. | HI>HCl>NH3 | C. | HCl>HI>NH3 | D. | NH3>HI>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
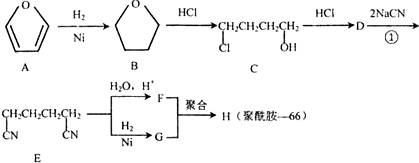
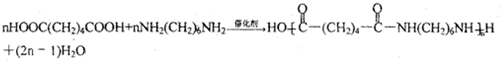 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{15}^{52}$P的原子核中含有15个中子 | |
| B. | ${\;}_{15}^{52}$P的相对原子质量为32 | |
| C. | ${\;}_{15}^{52}$P原子的质量数是17 | |
| D. | ${\;}_{15}^{52}$P原子中含有的电子数和质子数都是15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | Mg SO4 | NaBr |
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
| A. | CaSO4 | B. | MgSO4 | C. | NaCl | D. | MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 相对原子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊醇 | 130 | 0.8670 | 142 | 难溶 |
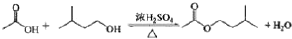
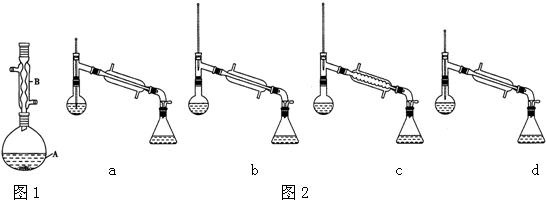
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
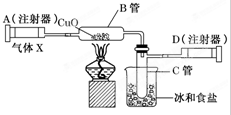 如图所示的实验装置可用来测定含两种元素的气体X的分子式.
如图所示的实验装置可用来测定含两种元素的气体X的分子式.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com