
����Ŀ����15�֣���̼���ʵļ�ֵ��ת���������ڡ���̼���Ϳɳ����Է�չ��������Ҫ���о���ֵ����ش��������⣺
��1����֪CO�����л�ѧ��ΪC��O����صĻ�ѧ�������������£�
��ѧ�� | H��O | C��O | C=O | H��H |
E/(kJ��mol1) | 463 | 1075 | 803 | 436 |
CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H=___________kJ��mol1���������������COƽ��ת���ʵĴ�ʩ��_______________�����ţ���
CO2(g)��H2(g) ��H=___________kJ��mol1���������������COƽ��ת���ʵĴ�ʩ��_______________�����ţ���
a������ѹǿ b�������¶�
c�����ԭ������H2O�ı��� d��ʹ�ø�Ч����
��2���ö��Ե缫���KHCO3��Һ���ɽ������е�CO2ת��Ϊ�����(HCOO)��Ȼ���һ�������Ƶ���Ҫ�л�����ԭ�ϼ��ᡣCO2������Ӧ�ĵ缫��ӦʽΪ________________������������ת��1 mol���ӣ���������������������״����Ϊ_________L��
��3���ұ���������ȡ����ϩ�ķ�ӦΪ��![]() (g)��CO2(g)
(g)��CO2(g)![]()
![]() (g)��CO(g)��H2O(g)���䷴Ӧ�������£�
(g)��CO(g)��H2O(g)���䷴Ӧ�������£�
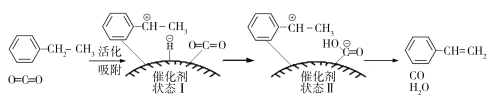
����ԭ�ϵ�״̬��____________��������ų��������ա�����
��һ���¶��£�������ܱ������г���2 mol�ұ���2 mol CO2����ʼѹǿΪp0��ƽ��ʱ���������������ʵ���Ϊ5 mol���ұ���ת����Ϊ_______����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=_______��[�����ѹ(p��)=������ѹ(p��)�������������]
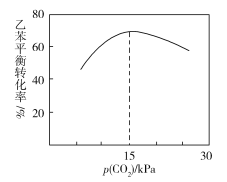
���ұ�ƽ��ת������p(CO2)�Ĺ�ϵ����ͼ��ʾ��������ұ�ƽ��ת��������p(CO2)�仯���仯��ԭ��________________________________________________��
���𰸡�41 bc 2CO2��2e��H2O===HCOO��![]() ��CO2��2e��H2O===HCOO��OH���������ɣ� 5.6 ���� 50% 0.25p0 ����CO2ѹǿ����CO2Ũ�������ұ�ƽ��ת��������CO2ѹǿ����������ɴ��������ұ����������½�
��CO2��2e��H2O===HCOO��OH���������ɣ� 5.6 ���� 50% 0.25p0 ����CO2ѹǿ����CO2Ũ�������ұ�ƽ��ת��������CO2ѹǿ����������ɴ��������ұ����������½�
��������
��1����H=463 kJ��mol1��2��1075 kJ��mol1803 kJ��mol1��2436 kJ��mol1=41 kJ��mol1��
��2��CO2ת��ΪHCOO�õ�2�����ӣ���OHƽ���ɣ��缫��ӦʽΪCO2��2e��H2O===HCOO��OH��2CO2��2e��H2O===HCOO��![]() ���������������������������ת��1 mol���ӣ������������������״����Ϊ5.6 L��
���������������������������ת��1 mol���ӣ������������������״����Ϊ5.6 L��
��3������ԭ�ϵ�״̬������ѧ���Ķ��ѣ���Ҫ����������
�����ұ���Ӧ��x mol��
![]() (g)��CO2(g)
(g)��CO2(g)![]()
![]() (g)��CO(g)��H2O(g)
(g)��CO(g)��H2O(g)
n0/mol 2 2 0 0 0
��n0/mol x x x x x
[n]/mol 2x 2x x x x
��ã�4��x=5
x=1
�ұ���ת����Ϊ![]() ��100%=50%
��100%=50%
ƽ���ѹǿΪ![]() ��p0=1.25 p0��Kp=
��p0=1.25 p0��Kp=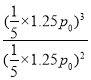 =0.25 p0
=0.25 p0
��һ����Χ�ڣ�p(CO2)Խ��˵����ԭ����CO2�����Խ�ߣ����ұ�ƽ��ת����Խ�ߣ��������������ڴ��������ϣ���CO2�ڴ������������ʹ���ʱ��������ұ��ڴ���������������½���ʹ�ұ�ƽ��ת��������p(CO2)������С��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᷨ�Ѱ��������ŷŵĺ��̷�ˮ(��Ҫ��������ΪMn2����Fe2����Al3��������������Ca2����Mg2����Cu2����Ni2��������)Ϊԭ�ϣ�����MnCO3�Ĺ����������£�
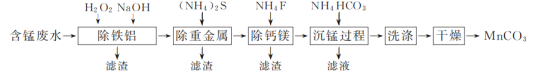
��֪��25 ��ʱ��Ksp(CaF2)��1.5��10��10��Ksp(MgF2)��7.5��10��11��
(1)�����к��̷�ˮ����ǰ����Ԥ�������õ���Ҫ����Mn2����ĸҺ��
�ٳ�����ʱ���ڽ����������ȼ���H2O2��Һ���ټ���NaOH��Һ����pH������H2O2��Һʱ������Ӧ�����ӷ���ʽΪ__________________________________________��
�ڳ���þ�����У���Ca2����Mg2��������ȫʱ����Һ��![]() ��________��
��________��
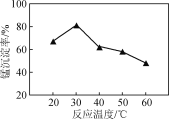
(2) ���̹�����pHΪ7.0�����³�ֽ��У���Ӧ�¶ȶ��̳����ʵ�Ӱ���ϵ��ͼ��ʾ��
�ٳ��̹��̷�����Ӧ�����ӷ���ʽΪ____________���ù����м����ʵ�������NH4HCO3��ԭ����________��
�ڵ��¶ȳ���30 �������̷�Ӧ���̳��������¶����߶��½���ԭ����______________________________��
(3) ���̺���˵õ�MnCO3�ֲ�Ʒ��������ȥ����ˮ����ˮ�Ҵ���ϴ��2��3�Σ��ٵ��¸���õ�������MnCO3������ˮ�Ҵ�ϴ�ӵ�Ŀ����____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ժ��ֱ�����ϵ�10mL���������50mL��������ȼ������CO2��Һ̬��H2O��ȼ�պ�������������Ϊ35mL����û�������Ϊ
A. C3H6 C4H6 B. C2H6 C3H6
C. C2H4 C3H8 D. C2H2 C2H6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��LDFCB������ӵ�ص�һ�ֵ���ʣ��õ������������ͬ����Ԫ��W��X��Y��Z����(����ͼ)��Y����������������X�ĺ����������������Ԫ������������֮��Ϊ20������˵����ȷ����( )
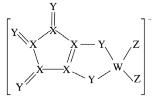
A.����Ԫ�صĵ����У�Z�ķе����
B.ԭ�Ӱ뾶��W��X��Y��Z
C.W��Z�γɵķ����и�ԭ�Ӿ�����8�����ȶ��ṹ
D.Y�ֱ�����������Ԫ���γɵĶ�Ԫ�������У�Y�ļ�̬��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1200��ʱ����Ȼ���������лᷢ�����з�Ӧ��
H2S��g��+3/2 O2��g���TSO2��g��+H2O��g�� ��H1
2H2S��g��+SO2��g���T3/2 S2��g��+2H2O��g�� ��H2
H2S��g��+1/2 O2��g���TS��g��+H2O��g�� ��H3
2S��g���TS2��g�� ��H4
���H4����ȷ����ʽΪ�� ��
A.��H4=3/2����H1-��H2-3��H3��B.��H4=2/3 ��3��H3-��H1-��H2��
C.��H4=3/2����H1+��H2-3��H3��D.��H4=2/3 ����H1+��H2-3��H3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�������Ȼ�ѧ��Ӧ����ʽ��
��1��1mol���������������Һ��Ӧ�ų�114.6kJ������д����ʾ�к��ȵ��Ȼ�ѧ��Ӧ����ʽ____________��
��2��0.5molC2H5OH��l����ȫȼ�շų�683.4kJ������д����ʾC2H5OHȼ�����Ȼ�ѧ��Ӧ����ʽ________��
��3��24g̼������H2O��g����Ӧ����262.6kJ����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ��������0.5molN2������˵������ȷ���ǣ� ��

A.��Ӧ����1molN2ʱת��4mole-
B.��Ӧ������֮�ʹ�������������֮��
C.N2O(g)+NO(g)=N2(g)+NO2(g) ��H=-139kJ��mol-1
D.�ϼ���������֮��С�ڳɼ��ͷ�����֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС����ݸ���֪ʶ������²ⶨ���ڼ�ȩ������װ��(�г�װ������)��
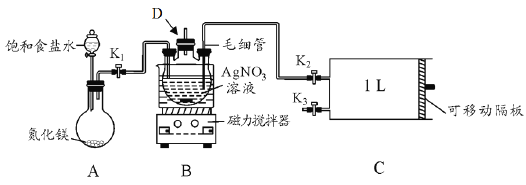
I������������Һ
(1)ʢװAgNO3��Һ������D������_________��
(2)�ر�K2��K3����K1�ͷ�Һ©��������������ʳ��ˮ���뵽Բ����ƿ�У����۲쵽D��������ɵİ�ɫ����ǡ����ȫ�ܽ�ʱ���ر�K1�ͷ�Һ©����������д��Aװ���з�����Ӧ�Ļ�ѧ����ʽ____������ʳ��ˮ����;��_______��
(3)��֪������Һ�ijɷ���Ag(NH3)2OH��д��D������������Һ�Ļ�ѧ����ʽ_________ ��
II���ⶨ���ڿ����м�ȩ����
(4)����ˮԡ����D����K3������������������˳鵽���Ҷˣ�����1L���ڿ������ر�K3������������___________�����ƽ�����������ʮ�Ρ�
(5)װ����ëϸ�ܵ�������_____________ ��
(6)��֪��ȩ��������Һ�����Ļ�ѧ����ʽΪHCHO+4Ag(NH3)2OH=(NH4)2CO3+4Ag��+6NH3��+2H2O����ù�����Ag 2.16mg��������м�ȩ�ĺ���Ϊ________mg L-1(�������������ʲ���������Һ��Ӧ)��
(7)�����װ�ô���һ�����ԵIJ���֮����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ԭ�����͵��ǣ� ��
A. ����������ȼ�յýϿ졢����ȫ
B. ʵ���ҿ����ñ���ʳ��ˮ�ռ�����
C. �ϳ�NH3��ӦΪ���ȷ�Ӧ��Ϊ���NH3�IJ��ʣ�Ӧ��ȡ�����¶ȵĴ�ʩ
D. ��H2��I2��HIƽ����ϵ��ѹ����������ɫ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com