
| A. | 溴苯 | B. | 对二甲苯 | C. | 丙炔 | D. | 丙烯 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A.溴苯是1个溴原子取代了苯分子中的1个H原子形成的,故溴苯分子中所有的原子也处于同一平面,故A正确;
B.对二甲苯(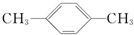 )是2个-CH3取代了苯分子中的2个H原子,因烷烃中C、H原子是四面体结构,故-CH3中C原子与3个H原子不可能全部处于同一平面,所以对二甲苯分子中所有原子不可能都处于同一平面,故B错误;
)是2个-CH3取代了苯分子中的2个H原子,因烷烃中C、H原子是四面体结构,故-CH3中C原子与3个H原子不可能全部处于同一平面,所以对二甲苯分子中所有原子不可能都处于同一平面,故B错误;
C.丙炔分子中也含有-CH3,故丙烯分子中所有原子不可能都处于同一平面,故C错误;
D.丙烯分子中也含有-CH3,故丙烯分子中所有原子不可能都处于同一平面,故D错误.
故选A.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,题目难度不大.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| 编号 | 实验操作 | 现象 | 解释或结论 |
| A | 在稀硝酸中加入过量的铁粉,充分反应后滴人KSCN溶液 | 溶液呈红色 | HNO3将Fe氧化为Fe3+ |
| B | 将苯、溴水混合后加入大试管加热 | 试管底部产生油状物 | 苯发生了取代反应生成了溴苯 |
| C | Cl2通人品红溶液中 | 溶液褪色 | Cl2具有漂白性 |
| D | KIO3溶液中加入HI溶液并加入淀粉 | 溶液变蓝色 | 氧化性:KIO3>I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 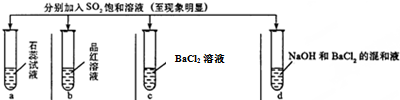 | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当混合气体的平均摩尔质量不再发生变化时,说明反应达到平衡状态 | |
| B. | 用X表示5 min内此反应的反应速率是(0.1-0.2a)mol•(L•min)-1 | |
| C. | 向平衡后的体系中加入l mol M,v(逆)增大,v(正)减小,平衡逆向移动 | |
| D. | 若平衡后再充入l mol X和(n+1)mol Y,再次达平衡时X的物质的量大于(2-2a)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解温度:CH4>H2S | B. | 氧化性:NaClO>Na2SO3 | ||
| C. | 同浓度溶液pH:Na2SiO3>Na2CO3 | D. | 金属性:Ca>Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
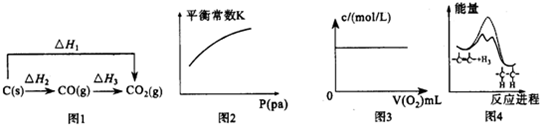 ( )
( )| A. | 图1中的△H1>△H2 | |
| B. | 对于可逆反应A(s)+3B(g)?2C(g)△H>0,压强对平衡常数K的影响符合图2 | |
| C. | 图3表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系 | |
| D. | 由图4可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com