
【题目】用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO33H2O2),它具有杀菌消毒去油污的能力且不会污染水源.
(1)写出H2O2的电子式 .
(2)这种洗涤剂中的双氧水可以将废水中的氰化钠(NaCN)转化为无毒物同时生成NH3 , 写出反应的离子方程式: .
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用.试分析其中的原因(结合文字表述和离子方程式说明): .
【答案】
(1)![]()
(2)H2O2+CN﹣+H2O=HCO3﹣+NH3
(3)Fe3+会加速H2O2分解,使洗涤剂失去杀菌作用,2H2O2 ![]() 2H2O+O2↑;Fe3+与CO32﹣水解相互促进,使洗涤剂失去去污能力,2Fe3++3CO32﹣+3H2O═2Fe(OH)3↓+3CO2↑
2H2O+O2↑;Fe3+与CO32﹣水解相互促进,使洗涤剂失去去污能力,2Fe3++3CO32﹣+3H2O═2Fe(OH)3↓+3CO2↑
【解析】解:(1)双氧水为共价化合物,分子中存在两个氧氢键和一个O﹣O键,双氧水的电子式为: ![]() ,所以答案是:
,所以答案是: ![]() ;(2)根据题目信息:这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成NH3 , 其中碳元素的化合价升高,则根据原子守恒可知无毒的物质是碳酸氢钠,结合原子守恒和电荷守恒,写出反应的离子方程式为:H2O2+CN﹣+H2O=HCO3﹣+NH3 , 所以答案是:H2O2+CN﹣+H2O=HCO3﹣+NH3;(3)双氧水因具有氧化性而具有杀菌消毒能力,但是2H2O2═2H2O+O2 , 铁离子会加速H2O2分解,使洗涤剂失去杀菌作用,此外,三价铁离子和纯碱中的碳酸根的水解双促进,2Fe3++3CO32﹣+3H2O═2Fe(OH)3↓+3CO2↑使洗涤剂失去去污能力,所以答案是:Fe3+会加速H2O2分解,使洗涤剂失去杀菌作用,2H2O2
;(2)根据题目信息:这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成NH3 , 其中碳元素的化合价升高,则根据原子守恒可知无毒的物质是碳酸氢钠,结合原子守恒和电荷守恒,写出反应的离子方程式为:H2O2+CN﹣+H2O=HCO3﹣+NH3 , 所以答案是:H2O2+CN﹣+H2O=HCO3﹣+NH3;(3)双氧水因具有氧化性而具有杀菌消毒能力,但是2H2O2═2H2O+O2 , 铁离子会加速H2O2分解,使洗涤剂失去杀菌作用,此外,三价铁离子和纯碱中的碳酸根的水解双促进,2Fe3++3CO32﹣+3H2O═2Fe(OH)3↓+3CO2↑使洗涤剂失去去污能力,所以答案是:Fe3+会加速H2O2分解,使洗涤剂失去杀菌作用,2H2O2 ![]() 2H2O+O2↑;Fe3+与CO32﹣水解相互促进,使洗涤剂失去去污能力,2Fe3++3CO32﹣+3H2O═2Fe(OH)3↓+3CO2↑.
2H2O+O2↑;Fe3+与CO32﹣水解相互促进,使洗涤剂失去去污能力,2Fe3++3CO32﹣+3H2O═2Fe(OH)3↓+3CO2↑.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】用石墨作电极电解下列溶液
①稀H2SO4②K2SO4溶液 ③NaCl溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1的是(填序号)_______。
(2)阴极、阳极都有气体产生,其中溶液pH变大的是________。(填序号)
(3)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小的是________ (填序号),其总反应的化学方程式是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写错误的是( )
A. 在蓝色的淀粉溶液中通入足量SO2后成无色溶液:I2+SO2+2H2O=2I-+SO42-+4H+
B. 饱和Na2CO3溶液中通入CO2足量:2Na++CO32-+ CO2+H2O=2NaHCO3↓
C. 向酸性KMnO4溶液中加入H2O2:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D. 钠投入CuSO4溶液中:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①pH=2的CH3COOH溶液;②pH=2的H2SO4溶液;③pH=12的氨水;④pH=12的NaOH溶液。室温条件下,有关上述溶液的比较中,正确的是( )
A. 水电离的c(H+):①=②=③=④
B. 将②、④溶液混合后,pH=7,消耗溶液的体积:②<④
C. 等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D. 向10 mL上述四溶液中各加入90 mL水后,溶液的pH:③>④>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在无色溶液中能大量共存的是( )
A. Fe3+、NH4+、OH-、Cl- B. Na+、H+、NO3-、SO42-
C. Fe2+、Fe3+、Na+、NO3- D. Fe2+、NH4+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET(聚对苯二甲酸乙二醇酯,简称聚酯)制作的。利用废聚酯饮料瓶制备对苯二甲酸的反应原理如下:
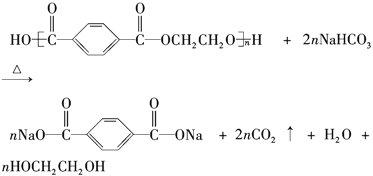
实验过程如下:
步骤1:在100mL四颈瓶上分别装置冷凝管、搅拌器和温度计。依次加入5g废饮料瓶碎片、0.05g氧化锌、5g碳酸氢钠和25mL乙二醇。缓慢搅拌,油浴加热,升温到180℃,反应15min。
步骤2:冷却至160℃停止搅拌,将搅拌回流装置改成搅拌、减压蒸馏装置,减压蒸馏。
步骤3:向四颈瓶中加入50mL沸水,搅拌使残留物溶解。抽滤除去少量不溶物。
步骤4:将滤液转移到400mL烧杯中,用25mL水荡洗滤瓶并倒入烧杯中,再添加水使溶液总体积达200mL,加入沸石,将烧杯置于石棉网上加热煮沸。
步骤5:取下烧杯,取出沸石后趁热边搅拌边用8~10mL1:1HCl酸化,酸化结束,体系呈白色浆糊状。
步骤6:冷至室温后再用冰水冷却。抽滤,滤饼用蒸馏水洗涤数次至滤出液pH=6,抽干后再用10mL丙酮分2次洗涤,抽干,干燥。
(1)步骤1反应过程中的现象是_________________________________________。
(2)步骤2是为了分离出________。
(3)步骤3抽滤需要用到的主要仪器有____________________________________。
(4)步骤4加沸石的目的是____________________________________________。
(5)步骤5用盐酸酸化的目的是__________________________________________。
(6)步骤6用丙酮洗涤的目的是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示有关物质之间的转化关系,A、C、E、G为非金属单质,其中A、G常温常压下为气态,E遇淀粉变蓝,K是一种常用食品添加剂,L是常见的无色无味液体,I为淡黄色固体,J的焰色反应呈浅紫色(透过蓝色钴玻璃)。
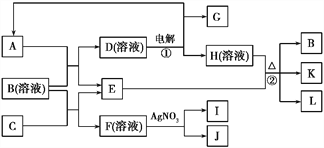
(1)B、I代表的物质化学式分别为__________、__________。
(2)写出反应①②的离子方程式:
①_________________________________________________;
②____________________________________________________________。
(3)选出实验室保存C单质的注意事项____________
A.无色瓶 B.棕色瓶 C.橡胶塞 D.玻璃塞
除此之外还采取了什么特殊保存方法:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“毒性气体”CO、NO及H2S可作为新型药物开发的潜在靶点,用以开发更多新型药物来帮助治疗多种人类疾病。下列有关这三种气体的说法正确的是( )
A.都是非电解质B.都易溶于水
C.都能与碱溶液反应D.都属于共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com