
| 滴定次数 | 待测液体的体积/mL | 标准碱溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 第一次 | 20.00mL | 0.00 | 20.98 |
| 第二次 | 20.00mL | 0.22 | 20.20 |
| 第三次 | 20.00mL | 0.36 | 20.38 |
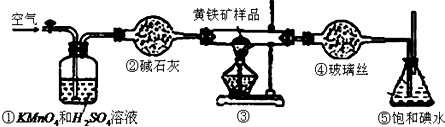
分析 (1)装置③中FeS2在加热条件下与氧气反应生成二氧化硫知氧化铁,根据元素守恒书写化学方程式;
(2)萃取、分液的主要仪器为分液漏斗,根据滴定生成的酸在水溶液中,所以需要取上层水溶液;
(3)装置①装有酸性高锰酸钾溶液,具有强氧化性,可氧化除去空气中的还原性气体,提高实验的准确率;
(4)装置④中玻璃丝的作用阻挡固体颗粒,得到平缓的二氧化硫气流;
(5)根据题意,用氢氧化钠滴定混合强酸溶液,所以常用的指示剂为酚酞,在滴定终点时溶液变为浅红色;
(6)对于多次测量数据一般要求平均值进行数据处理,由于第一次所消耗标准液的体积与后两次相关较大,为减小误差,只求后两次标准液的体积的平均值:20.00ml,根据反应4FeS2+11O2=2Fe2O3+8SO2,I2+SO2+2H2O=2HI+H2SO4,H++OH-═H2O,得关系式S~SO2~4H+~4OH-,所以样品中硫元素的质量为:$\frac{0.020L×0.20mol/L}{4}$mol×32g/mol×$\frac{300ml}{20ml}$=0.48g,据此计算样品中硫元素的质量分数;
(7)装置⑤所得溶液为HI、H2SO4的混合溶液,为测得硫的质量分数,最好选用能与SO42-反应生成不溶于酸性溶液的沉淀.
解答 解:(1)装置③中FeS2在加热条件下与氧气反应生成二氧化硫知氧化铁,反应的化学方程式为4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2,
故答案为:4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2;
(2)萃取、分液的主要仪器为分液漏斗,因为CCl4密度大于水,所以萃取碘后,有机层在下层,水溶液为上层,则后续滴定生成的酸在水溶液中,所以需要取上层水溶液,故答案为:分液漏斗;上;
(3)装置①装有酸性高锰酸钾溶液,具有强氧化性,可氧化除去空气中的还原性气体,提高实验的准确率,
故答案为:除去空气中的还原性气体,提高实验的准确率;
(4)装置④中玻璃丝的作用是过滤二氧化硫气体避免氧化铁颗粒进入,得到平缓的二氧化硫气流,
故答案为:过滤二氧化硫气体避免氧化铁颗粒进入,得到平缓的二氧化硫气流;
(5)根据题意,用氢氧化钠滴定混合强酸溶液,所以常用的指示剂为酚酞,当滴入最后一滴NaOH溶液后,溶液变为浅红色,并在半分钟内不褪色,说明滴定已经达到终点,
故答案为:酚酞;滴入最后一滴NaOH溶液后,溶液变为浅红色,并在半分钟内不褪色;
(6)对于多次测量数据一般要求平均值进行数据处理,由于第一次所消耗标准液的体积与后两次相关较大,为减小误差,只求后两次标准液的体积的平均值:20.00ml,根据反应4FeS2+11O2=2Fe2O3+8SO2,I2+SO2+2H2O=2HI+H2SO4,H++OH-═H2O,得关系式S~SO2~4H+~4OH-,所以样品中硫元素的质量为:$\frac{0.020L×0.20mol/L}{4}$mol×32g/mol×$\frac{300ml}{20ml}$=0.48g,所以样品中硫元素的质量分数为$\frac{0.48}{2.0}$×100%=24.0%,
故答案为:24.0%;
(7)装置⑤所得溶液为HI、H2SO4的混合溶液,为测得硫的质量分数,最好选用能与SO42-反应生成不溶于酸性溶液的沉淀,即氯化钡符合题意,故选B,
故答案为:B.
点评 本题考查了利用二氧化硫的性质测定黄铁矿中硫的质量分数,涉及化学方程式的书写、气体除杂、滴定实验指示剂的选择以及计算等,考查知识点较多,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:推断题
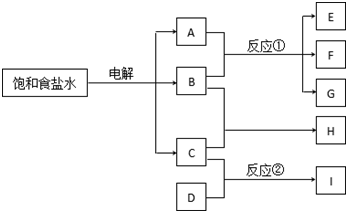 下列每一方框中的字母代表一种反应物或生成物:
下列每一方框中的字母代表一种反应物或生成物:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 双键、三键中一定含有π键 | |
| B. | 成键原子间原子轨道重叠越多,共价键越牢固 | |
| C. | 因每个原子未成对电子数是一定的,故配对原子个数也一定 | |
| D. | 每一个原子轨道在空间都具有方向性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
 或
或 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2与C2H4 | B. | CO与C2H4 | C. | CO 与C3H6 | D. | H2与C4H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水中溶解性:Na2CO3<NaHCO3 | |
| B. | 热稳定性:Na2CO3<NaHCO3 | |
| C. | 同浓度溶液与足量酸反应产生气体的速度:Na2CO3<NaHCO3 | |
| D. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HF>HCl>HBr>HI | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性:H2SO4>H3PO4>HClO4 | D. | 氧化性:O2>S>Se |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,18g重水(D2O)中所含的电子数为10 NA | |
| B. | 标准状况下,14g氮气含有的核外电子数为5NA | |
| C. | 标准状况下,22.4L氢气和氯气的混合气体中含有的分子总数为NA | |
| D. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片能和硫酸铜溶液反应 | |
| B. | 铝片能和氢氧化钠溶液反应 | |
| C. | 铝片不能和硝酸反应 | |
| D. | 铝片表面能形成具有保护作用的氧化膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com