
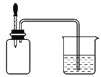
【题目】为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶,F是用于鼓入空气的打气球。

(1)实验时,第一步实验操作为:将装有CaCO3干燥管下移与稀硝酸反应生成CO2,该操作的作用是_____。
(2)第二步,提起干燥管B,将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为________。有人认为E中收集到的可能是H2而不是NO,如何证明?_______________。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。请指出不当之处是__________。
(4)将一支试管中充入20mLNO2和O2的混合气体,倒扣在水槽中,待反应停止后,试管内剩余2mL无色气体。则原混合气体中NO2的体积是______mL。
【答案】 除去E中的空气,防止对NO检验造成干扰 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 挤压F向E中鼓入空气,E内气体由无色变成红棕色,证明收集到的气体是NO E中左导管长右导管短,不利于排尽空气 17.2或14.4
【解析】(1)实验时,可先将B装置中CaCO3放入硝酸中,碳酸钙和硝酸反应生成二氧化碳气体,先排出去其中的空气,以便在E烧瓶中收集到NO,以便观察颜色;因此该操作的作用是除去E中的空气,防止对NO检验造成干扰;(2)稀硝酸与铜反应生成硝酸铜、水和NO,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;A中硝酸和铜反应生成NO,易与氧气反应,则将F气球中空气压入E中,有红棕色气体生成,如观察到红棕色,则说明生成NO而不是氢气;(3)在未鼓入空气的情况下,E中就产生红棕色,说明空气没有完全被排尽,根据装置图可知是由于E中左导管长右导管短,不利于排尽空气;(4)设混合气体中NO2是x mL,氧气是y mL,则x+y=20。如果剩余的气体是氧气,则根据反应方程式4NO2+O2+2H2O=4HNO3可知消耗的氧气是0.25x mL,则0.25x+2=y,解得x=14.4、y=5.6;如果剩余气体是NO,则根据方程式3NO2+H2O=2HNO3+NO可知剩余NO2是6mL,则4y+6=x,解得x=17.2、x=2.8。


科目:高中化学 来源: 题型:
【题目】一定温度下,将2molSO2和1molO2充入2L密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mo!,下列说法中正确的是
2SO3(g) △H=-197kJ/mo!,下列说法中正确的是
A. 反应达到平衡状态时,会放出197kJ的热量
B. 增大O2浓度可以使SO2转化率达到100%
C. 使用合适的催化剂、升高温度均可加大反应速率
D. 反应达到平衡时,正反应和逆反应的化学反应速率相等且不为零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,满足下列条件的溶液一定呈酸性的是( )
A.能与金属Al反应放出H2的溶液
B.加酚酞后显无色的溶液
C.pH=6的某溶液
D.c(H+)>c(OH﹣)的任意水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z三元素的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体, D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。各物质之间的转换关系如下图,部分生成物省略。请回答下列问题:

(1)写出A的化学式__________________,C的电子式______________________,
D的结构式______________________________。
(2)将22.4L(标准状况)D气体通入1L 1mol/L NaOH溶液中,完全吸收后,溶液中除了Na+外,还大量存在的离子是______________________________。
(3)已知M溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的离子方程式___________________________________________________________。
(4)检验化合物K中阳离子的实验方法是______________________________________
(5)写出反应K+G→L的化学方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值,下列说法正确的是
A. 1 mol Cu和2 mol热浓硫酸反应,生成的SO2分子数目为NA
B. 由H2O2制得2.24 L O2,转移的电子数目为0.2NA
C. 常温常压下,8 g O2与O3的混合气体中含有4NA个电子
D. 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓H2SO4 密度1.84g/mL,物质的量浓度为18.4mol/L,质量分数为98%,取10mL浓H2SO4和a mL水混合得物质的量浓度为C mol/L,质量分数为b%.下列组合正确的是( ) (i)若C=9.2则a>10 b>49% (ii)若C=9.2则a>10 b<49%
(iii)若b=49则a=18.4 C<9.2 (iv)若b=49则a=18.4 C>9.2.
A.(i)(iii)
B.(i)(iv)
C.(ii)(iii)
D.(ii)(iv)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )
①CO、O2 ②Cl2、CH4 ③NO2、O2 ④N2、H2
A. ①② B. ②④ C. ③④ D. ②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com