
 .
.分析 A、B、C、D、E是位于短周期的主族元素,
③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小,A、B分别位于第IA族、第IIIA族;
④A与B质子数之和是D质子数的3倍,只有A是Na、B是Al、D是O元素才符合A与B质子数之和是D质子数的3倍,所以A是Na元素、B是Al元素、D是O元素;
①C、D同主族且热稳定性:HmD>HmC,则C是S元素;
②Cm-、E(m-1)-具有相同的电子层结构,则E是Cl元素,且m=2;
再结合题目分析解答.
解答 解:A、B、C、D、E是位于短周期的主族元素,
③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小,A、B分别位于第IA族、第IIIA族;
④A与B质子数之和是D质子数的3倍,只有A是Na、B是Al、D是O元素才符合A与B质子数之和是D质子数的3倍,所以A是Na元素、B是Al元素、D是O元素;
①C、D同主族且热稳定性:HmD>HmC,则C是S元素;
②Cm-、E(m-1)-具有相同的电子层结构,则E是Cl元素,且m=2;
(1)S2-的核内有16个质子、核外有3个电子层、最外层电子数为8,则该离子电子层结构示意图为 ,故答案为:
,故答案为: ;
;
(2)元素的非金属性越强,其简单阴离子的还原性越弱,非金属性Cl>S,则S2-、Cl-的还原性强弱顺序为:Cl->S2-,氯气能氧化硫化钠生成S,能证明其还原性强弱的离子方程式为Cl2+S 2-=2Cl-+S↓,
故答案为:Cl->S2-;Cl2+S 2-=2Cl-+S↓;
(3)E的单质是氯气,A、D形成的化合物水溶液是NaOH溶液,二者反应生成NaCl、NaClO和水,其离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,
故答案为:2OH-+Cl2=Cl-+ClO-+H2O;
(4)A、B、C、E、D单质分别是Na、Al、S、Cl2、O2,
Na和氧气反应生成氧化钠、氧化钠被氧化生成过氧化钠、过氧化钠和水反应生成NaOH和氧气,符合转化关系;
Al和氧气反应生成氧化铝,氧化铝不能和氧气反应,所以不符合转化关系;
S和氧气反应生成二氧化硫、二氧化硫被氧化生成三氧化硫、三氧化硫和水反应生成硫酸,符合转化关系;
氯气和氧气不反应,不符合转化关系;
符合转化关系的是Na、S,
故答案为:Na、S.
点评 本题考查位置结构性质相互关系及运用,涉及元素推断、元素化合物之间转化、离子方程式书写、氧化性强弱比较等知识点,明确原子结构、元素周期表结构及元素化合物性质是解本题关键,侧重考查学生分析推断及知识综合运用能力,题目难度不大.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:解答题
 利用Fe+CuSO4=Cu+FeSO4设计一个原电池.画出实验装置图. 并指出:
利用Fe+CuSO4=Cu+FeSO4设计一个原电池.画出实验装置图. 并指出:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
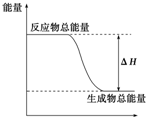
| A. | 铝热反应 | B. | 灼热的炭与二氧化碳反应 | ||
| C. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合 | D. | 碳酸钙的分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,在B分子中Y原子的杂化方式为sp3,B中O-Y-H的键角小于(填“大于”“等于”或“小于”)A中O-Y-H键角.
,在B分子中Y原子的杂化方式为sp3,B中O-Y-H的键角小于(填“大于”“等于”或“小于”)A中O-Y-H键角.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 、
、
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g CH4中含有4NA个C-H键 | |
| B. | 1L mol•L-1CH3COOH溶液中含有0.1NA个H+ | |
| C. | 标准状况下的22.4L辛烷完全燃烧,生成CO2分子数为8NA | |
| D. | 1mol 乙炔中含有的电子数为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K正反应=K逆反应 | B. | K正反应>K逆反应 | ||
| C. | K正反应<K逆反应 | D. | K正反应×K逆反应=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: | B. | NH4Cl的电子式: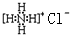 | ||
| C. | F原子的结构示意图: | D. | 中子数为20的氯原子${\;}_{17}^{37}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将过量CO2气体通入水玻璃中可制得硅酸和纯碱 | |
| B. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移电子0.1 mol | |
| C. | 1 L 2 mol•L-1明矾经水解可得到氢氧化铝胶体粒子数目为2×6.02×1023 | |
| D. | 漂白粉溶于水能导电,故漂白粉是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com