
分析 (1)碘不易溶于水,易溶于有机溶剂;
(2)水与汽油分层;
(3)CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物,互溶但沸点不同.
解答 解:(1)碘不易溶于水,易溶于有机溶剂,则利用萃取分液法,然后蒸馏从碘水中分离出碘,
故答案为:A;
(2)水与汽油分层,则利用分液法分离水和汽油的混合物,
故答案为:C;
(3)CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物,互溶但沸点不同,则利用蒸馏法分离,
故答案为:D.
点评 本题考查物质的分离、提纯方法及选择,为高频考点,把握物质的性质及分离原理为解答的关键,注意物质性质差异及分离方法的选择,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
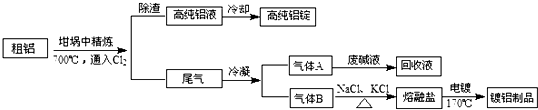
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
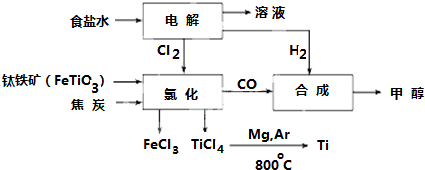
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2NH3+3CuO→3Cu+N2+3H2O | B. | 2Na+2NH3→2NaNH2+H2↑ | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)和(6) | B. | (3)和(4) | C. | (2)和(4) | D. | (2)和(5) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com