


 Ē§ĄļĀķ×ßĻņ¼ŁĘŚĘŚÄ©·ĀÕęŹŌ¾ķŗ®¼ŁĻµĮŠ“š°ø
Ē§ĄļĀķ×ßĻņ¼ŁĘŚĘŚÄ©·ĀÕęŹŌ¾ķŗ®¼ŁĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| c2(NH3) |
| c(N2)c3(H2) |
| c2(NH3) |
| c(N2)c3(H2) |
| 1 |
| 12 |
| 1 |
| 12 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā

¢ŁÉč¼Ę¼××°ÖƵÄÄæµÄŹĒ_________________”£¼××°ÖĆ__________£ØĢī”°ÄÜ”±»ņ”°²»ÄÜ”±£©ÓĆŅŅ×°ÖĆĄ““śĢę”£
¢Ś×°ÖĆŅŅÖŠŹ¢ÓŠµÄŅŗĢåŹĒ__________£¬øĆ×°ÖĆæÉæ“×÷ŹĒŅ»øö___________£ØĢīijŅĒĘ÷Ćū³Ę£©”£
£Ø2£©ŌŚµŖµÄ»ÆŗĻĪļÖŠ£¬ÓŠŅ»ĄąŃĪ½ŠŃĒĻõĖįŃĪ£¬ČēŃĒĻõĖįÄĘ£ØNaNO2£©µČ”£NaNO2ŹĒŅ»ÖÖĒ±ŌŚµÄÖĀ°©ĪļÖŹ£¬¹żĮæ»ņ³¤ĘŚŹ¹ÓĆ»į¶ŌČĖ²śÉśĪ£ŗ¦”£ÓÉÓŚŃĒĻõĖįÄĘÓŠĻĢĪ¶£¬Ķā¹ŪÓėNaClĻąĖĘ£¬Ōų¶ą“Ī·¢Éś¹ż±»Ī󵱏³ŃĪŹ¹ÓƵďĀ¼ž”£ŅŃÖŖ£ŗHNO2ŹĒŅ»ÖÖČõĖį£¬²»ĪČ¶Ø£¬Ņ×·Ö½āÉś³ÉNOŗĶNO2£»ĖüÄܱ»³£¼ūµÄĒæŃõ»Æ¼ĮŃõ»Æ£»ŌŚĖįŠŌČÜŅŗÖŠĖüŅ²ŹĒŅ»ÖÖŃõ»Æ¼Į£¬ČēÄÜ°ŃI-Ńõ»Æ³ÉI2;AgNO2ŹĒŅ»ÖÖÄŃČÜÓŚĖ®Ņ×ČÜÓŚĖįµÄ»ÆŗĻĪļ”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁČĖĢåÕż³£µÄŃŖŗģµ°°×ÖŠÓ¦ŗ¬Fe2+”£ČōĪóŹ³ŃĒĻõĖįŃĪ£ØČēNaNO2£©£¬Ōņµ¼ÖĀŃŖŗģµ°°×ÖŠFe2+×Ŗ»ÆĪŖFe3+¶ųÖŠ¶¾£¬·žÓĆĪ¬ÉśĖŲCæɽā¶¾”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ_____________”£
A.ŃĒĻõĖįŃĪŹĒ»¹Ō¼Į B.Ī¬ÉśĖŲCŹĒ»¹Ō¼Į
C.Ī¬ÉśĖŲC½«Fe3+»¹ŌĪŖFe2+ D.ŃĒĻõĖįŃĪ±»»¹Ō
¢ŚĻĀĮŠĖµ·ØÖŠ£¬ÄÜÓĆĄ“Ēų±šNaNO2ŗĶNaClµÄŹĒ______________”£
A.²ā¶ØÕāĮ½ÖÖČÜŅŗµÄpH
B.ÓĆAgNO3ŗĶHNO3Į½ÖÖŹŌ¼ĮĄ“Ēų±š
C.ŌŚĖįŠŌĢõ¼žĻĀ¼ÓČėKIµķ·ŪŹŌŅŗĄ“Ēų±š
¢Ū°ŃŠĀÖĘĀČĘųĶØČėµ½NaNO2ČÜŅŗÖŠ£¬ĀČĖ®ĶŹÉ«£¬Éś³ÉNaNO3ŗĶHCl£¬ĒėŠ“³ö“Ė·“Ó¦µÄĄė×Ó·½³ĢŹ½______________”£
¢ÜĪŖĮĖ²ā¶ØÄ³ŃłĘ·ÖŠNaNO2µÄŗ¬Į棬æÉŅŌŹ¹ÓƱź×¼?KMnO4?ČÜŅŗ½ųŠŠµĪ¶Ø£¬ŹŌ»Ų“š£ŗKMnO4ČÜŅŗŌŚµĪ¶Ø¹ż³ĢÖŠ×÷____________£ØĢī”°Ńõ»Æ¼Į”±»ņ”°»¹Ō¼Į”±£©£¬øƵĪ¶Ø¹ż³Ģ_____________£ØĢī”°ŅŖ”±»ņ”°²»ŅŖ”±£©Įķ¼ÓÖøŹ¾¼Į”£
¢ŻŅŃÖŖHNO2µÄĖįŠŌ±Č“×ĖįĀŌĒ棬ijĶ¬Ń§ŌŚ¼ŅÖŠ½ųŠŠ¼ų±šNaNO2ÓėNaClµÄŹµŃ飬µ«Ėū¼ŅÖŠÖ»ÓŠÅØ“×Ėį£¬ĒėĪŹøĆŹµŃéÄÜ·ń³É¹¦£æ____________£ØĢī”°ÄÜ”±»ņ”°²»ÄÜ”±£©£¬ĒėĖµĆ÷ĄķÓÉ_______
_____________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2010Äź±±¾©ĪåÖŠø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌĢā ĢāŠĶ£ŗĢīæÕĢā
(12·Ö)ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ唣ĘäŌĄķĪŖ£ŗ
N2(g)+3H2(g)  2NH3(g) ”÷H= -92.4KJ/mol £¬¾Ż“Ė»Ų“šŅŌĻĀĪŹĢā£ŗ
2NH3(g) ”÷H= -92.4KJ/mol £¬¾Ż“Ė»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦ĖŁĀŹµÄŠšŹö£¬ÕżČ·µÄŹĒ£ØŃ”ĢīŠņŗÅ£© ”£
a£®ÉżøßĪĀ¶ČæÉŅŌŌö“ó»ī»Æ·Ö×Ó°Ł·ÖŹż£¬¼Óæģ·“Ó¦ĖŁĀŹ
b£®Ōö“óŃ¹Ēæ²»ÄÜŌö“ó»ī»Æ·Ö×Ó°Ł·ÖŹż£¬ĖłŅŌ²»æÉŅŌ¼Óæģ·“Ó¦ĖŁĀŹ
c£®Ź¹ÓĆ“ß»Æ¼ĮæÉŅŌŹ¹·“Ó¦Īļ·Ö×ÓĘ½¾łÄÜĮæÉżøߣ¬¼Óæģ·“Ó¦ĖŁĀŹ
d£®ŌŚÖŹĮæŅ»¶ØµÄĒéæöĻĀ£¬“߻ƼĮæÅĮ£µÄ±ķĆ껿“󊔣¬¶Ō·“Ó¦ĖŁĀŹÓŠĻŌÖųÓ°Ļģ
£Ø2£©¢ŁøĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖK=_______________________”£
¢Śøł¾ŻĪĀ¶Č¶Ō»ÆŃ§Ę½ŗāµÄÓ°Ļģ¹ęĀÉæÉÖŖ£¬¶ŌÓŚøĆ·“Ó¦£¬ĪĀ¶ČŌ½øߣ¬ĘäĘ½ŗā³£ŹżµÄÖµŌ½_____ ”£
£Ø3£©Ä³ĪĀ¶ČĻĀ£¬Čō°Ń10 mol N2Óė30 mol H2 ÖĆÓŚĢå»żĪŖ10 LµÄĆܱÕČŻĘ÷ÄŚ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬²āµĆĘ½ŗā»ģŗĻĘųĢåÖŠ°±µÄĢå»ż·ÖŹżĪŖ20%£¬ŌņøĆĪĀ¶ČĻĀ·“Ó¦µÄK=___________£ØæÉÓĆ·ÖŹż±ķŹ¾£©”£ÄÜĖµĆ÷øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ £ØĢī×ÖÄø£©”£
a£®ČŻĘ÷ÄŚµÄĆܶȱ£³Ö²»±ä b£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
c£®¦ŌÕż£ØN2£©£½2¦ŌÄę£ØNH3£© d£®»ģŗĻĘųĢåÖŠ c£ØNH3£©²»±ä
£Ø4£©¶ŌÓŚŗĻ³É°±·“Ó¦¶ųŃŌ£¬ĻĀĮŠÓŠ¹ŲĶ¼ĻóŅ»¶ØÕżČ·µÄŹĒ£ØŃ”ĢīŠņŗÅ£©_____________”£
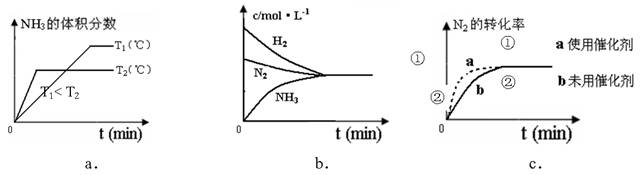
£Ø5£©ĻąĶ¬ĪĀ¶ČĻĀ£¬ÓŠŗćČŻĆܱÕČŻĘ÷AŗĶŗćŃ¹ĆܱÕČŻĘ÷B£¬Į½ČŻĘ÷ÖŠ¾ł³äČė1mol N2ŗĶ3 molH2£¬“ĖŹ±Į½ČŻĘ÷µÄĢå»żĻąµČ”£ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬AÖŠNH3µÄĢå»ż·ÖŹżĪŖa£¬·Å³öČČĮæQ1 kJ£»
BÖŠNH3µÄĢå»ż·ÖŹżĪŖb£¬·Å³öČČĮæQ2 kJ”£Ōņ£ŗa_____b(Ģī>”¢=”¢<)£¬ Q1_____ Q2(Ģī>”¢=”¢<)£¬ Q1_____92.4(Ģī>”¢=”¢<)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012½ģɽĪ÷Ź”ø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ唣ĘäŌĄķĪŖ£ŗ
N2(g)+3H2(g)  2NH3(g) ”÷H= -92.4KJ/mol
£¬¾Ż“Ė»Ų“šŅŌĻĀĪŹĢā£ŗ
2NH3(g) ”÷H= -92.4KJ/mol
£¬¾Ż“Ė»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦ĖŁĀŹµÄŠšŹö£¬ÕżČ·µÄŹĒ£ØŃ”ĢīŠņŗÅ£© ”£
a£®ÉżøßĪĀ¶ČæÉŅŌŌö“ó»ī»Æ·Ö×Ó°Ł·ÖŹż£¬¼Óæģ·“Ó¦ĖŁĀŹ
b£®Ōö“óŃ¹Ēæ²»ÄÜŌö“ó»ī»Æ·Ö×Ó°Ł·ÖŹż£¬ĖłŅŌ²»æÉŅŌ¼Óæģ·“Ó¦ĖŁĀŹ
c£®Ź¹ÓĆ“ß»Æ¼ĮæÉŅŌŹ¹·“Ó¦Īļ·Ö×ÓĘ½¾łÄÜĮæÉżøߣ¬¼Óæģ·“Ó¦ĖŁĀŹ
d£®ŌŚÖŹĮæŅ»¶ØµÄĒéæöĻĀ£¬“߻ƼĮæÅĮ£µÄ±ķĆ껿“󊔣¬¶Ō·“Ó¦ĖŁĀŹÓŠĻŌÖųÓ°Ļģ
£Ø2£©¢ŁøĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖK=_______________________”£
¢Śøł¾ŻĪĀ¶Č¶Ō»ÆŃ§Ę½ŗāµÄÓ°Ļģ¹ęĀÉæÉÖŖ£¬¶ŌÓŚøĆ·“Ó¦£¬ĪĀ¶ČŌ½øߣ¬ĘäĘ½ŗā³£ŹżµÄÖµŌ½_____ ”£
£Ø3£©Ä³ĪĀ¶ČĻĀ£¬Čō°Ń10 mol N2Óė30 mol H2 ÖĆÓŚĢå»żĪŖ10 LµÄĆܱÕČŻĘ÷ÄŚ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬²āµĆĘ½ŗā»ģŗĻĘųĢåÖŠ°±µÄĢå»ż·ÖŹżĪŖ20%£¬ŌņøĆĪĀ¶ČĻĀ·“Ó¦µÄK=___________£ØæÉÓĆ·ÖŹż±ķŹ¾£©”£ÄÜĖµĆ÷øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ_________ £ØĢī×ÖÄø£©”£[Ą“Ō“:ѧ*æĘ*ĶųZ*X*X*K]
a£®ČŻĘ÷ÄŚµÄĆܶȱ£³Ö²»±ä b£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
c£®¦ŌÕż£ØN2£©£½2¦ŌÄę£ØNH3£© d£®»ģŗĻĘųĢåÖŠ c£ØNH3£©²»±ä
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com