
15.用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H= +64.39kJ·mol-1
②2H2O2(l)=2H2O (l)+O2(g) △H= -196.46kJ·mol-1
③H2(g)+O2(g)=H2O(l) △H= -285.84kJ·mol-1
下列有关说法错误的是( )
A.铜可以溶解于稀盐酸与H2O2的混合溶液
B.铜溶解于酸性双氧水的热化学方程式为:
Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) △H= —319.68 kJ·mol-1
C.反应①是在任何条件下都不可能发生的化学反应
D.用H2O2和H2SO4的混合溶液溶解铜比用浓硫酸溶解铜环保
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 原子最外层电子数是次外层的三倍 |
| Z | 单质及其化合物的焰色反应为黄色 |
| W | W元素基态原子的M层全充满,N层只有一个电子 |
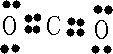
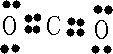
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率 (×10-3 mol?L-1?min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 17Cv |
| 200ρ |
| 17Cv |
| 200ρ |
| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | 取适量碘化钾淀粉溶液、稀硫酸于试管中,滴入过氧化氢溶液.(或:取适量饱和硫化氢溶液于试管中,滴入过氧化氢溶液.) | 溶液变蓝色 溶液变蓝色 .(或: 产生淡黄色沉淀或溶液变浑浊 产生淡黄色沉淀或溶液变浑浊 ) |
| 验证热不稳定性 | 取适量过氧化氢溶液于试管中, 稍微加热 稍微加热 用带火星的木条检验 用带火星的木条检验 . |
产生气泡,带火星的木条复燃. |
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率 (×10-3mol?L-1?min-1) |
7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
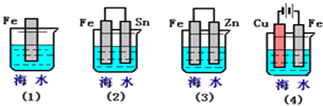
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com