
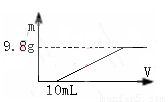
过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5 mol·L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为
A.0.05mol B.0.1mol
C.0.2mol D.0.25mol
D
【解析】
试题分析:铜与稀硝酸反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.由于硝酸过量,加入的氢氧化钠溶液首先和过量的硝酸反应生成硝酸钠,然后再与硝酸铜溶液反应产生氢氧化铜沉淀。反应后的溶液为硝酸铜和硝酸钠混合液。与硝酸反应消耗的氢氧化钠为10ml,所以硝酸钠中硝酸根离子为:n((NO3-)=n(Na+)=0.01×5 mol∕L=0.05 mol.n(Cu)=m∕M=6.4g∕64(g∕mol)=0.1mol. n{Cu(NO3)2}=0.1mol,硝酸铜中的硝酸根离子的物质的量为:=0.1mol×2=0.2mol.n((NO3-)总=0.2mol+0.05 mol=0.25 mol。选项为:D。
考点:考查 硝酸的化学性质及溶液中离子的物质的量的应该计算的知识。


科目:高中化学 来源: 题型:阅读理解
| 5.6-1.4 |
| 56 |
| 32.29 |
| 143.5 |
| n(Fe) |
| n(Cl) |
| 1 |
| 3 |
| 5.6-1.4 |
| 56 |
| 32.29 |
| 143.5 |
| n(Fe) |
| n(Cl) |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.84L | B、6.72L | C、4.48L | D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com