
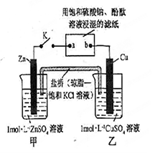
A.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| B.片刻后可观察到滤纸b点变红色 |
| C.片刻后甲池中c(SO42-)增大 |
D. 电极上发生还原反应 电极上发生还原反应 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
 Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
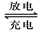 2PbSO4+2H2O
2PbSO4+2H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.放电时,负极质量增加 |
| B.充电时,应将外接直流电源的正极与蓄电池的铅电极相接 |
C.放电时,正极反应为: |
| D.铅蓄电池做电源电解Na2SO4溶液时,当有lmolO2产生时,消耗4molH2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

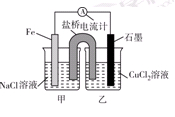
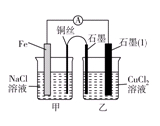
| A.甲中铁被保护不会腐蚀 |
| B.甲中正极反应式为4OH--4e- = 2H2O+O2 |
| C.乙中铁电极上发生氧化反应 |
| D.乙中石墨电极附近滴几滴碘化钾淀粉溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
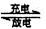 VO2++2H++V2+。下列叙述正确的是 ( )
VO2++2H++V2+。下列叙述正确的是 ( )| A.充电时阳极附近溶液的酸性减弱 |
| B.充电时阳极反应式为:VO2++2H++e-=VO2++H2O |
| C.放电过程中电解质溶液中阳离子移向负极 |
| D.放电时每转移1mol电子,负极有1mol V2+被氧化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
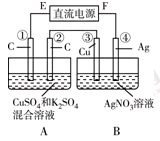
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在原电池中,化学能转变为电能,电子沿导线由正极流向负极 |
| B.双液原电池通过盐桥连接,KCl盐桥中K+朝正极定向迁移 |
| C.在电解池中,与电源负极相连的电极称为阳极,溶液中阴离子朝阳极定向迁移 |
| D.电解氯化铜溶液,在阴极上产生的气体能使湿润的KI-淀粉试纸变蓝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。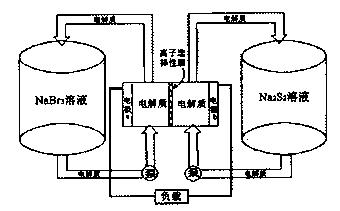
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com