
| A、分子式为C3H8与C6H14的两种有机物一定互为同系物 |
| B、对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
| C、分子式C4H10表示的物质必是纯净物 |
D、有机物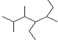 的名称:2,3,5-三甲基-4-乙基庚烷 的名称:2,3,5-三甲基-4-乙基庚烷 |
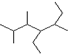 为烷烃的键线式,根据烷烃的命名原则进行命名.
为烷烃的键线式,根据烷烃的命名原则进行命名. 为烷烃,主链最长碳链含有7个C,主链为庚烷,编号从左端开始,在2、3、5号C原子上各含有1个甲基,在4号C含有1个乙基,该有机物名称为2,3,5-三甲基-4-乙基庚烷,故D正确;
为烷烃,主链最长碳链含有7个C,主链为庚烷,编号从左端开始,在2、3、5号C原子上各含有1个甲基,在4号C含有1个乙基,该有机物名称为2,3,5-三甲基-4-乙基庚烷,故D正确;

科目:高中化学 来源: 题型:
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe(OH)2 | 7.0 | 9.0 |
| Fe(OH)3 | 1.9 | 3.2 |
| Cr(OH)3 | 6.0 | 8.0 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | Z | |
| A | FeCl2溶液 | FeCl3 | KSCN溶液 |
| B | Fe粉 | A1粉 | NaOH溶液 |
| C | Fe2(SO4)3溶液 | FeSO4 | C12 |
| D | FeCl3溶液 | CuCl2 | Fe粉 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一氧化碳在高温下可还原硫酸钙,相关反应的平衡常数的对数与反应温度的关系如图所示.
一氧化碳在高温下可还原硫酸钙,相关反应的平衡常数的对数与反应温度的关系如图所示.| 1 |
| 4 |
| 1 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| CO? | H? | CH?OH | H?O |
| 0.7mol?L-1 | 0.5mol?L-1 | 0.3mol?L-1 | 0.3mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中有Fe2+、Cu2+ |
| B、剩下的固体是Fe和Cu |
| C、溶液中有Fe3+、Fe2+ |
| D、剩下的固体是Fe,无Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向饱和的碳酸钠溶液中通入CO2气体,没有明显实验现象 |
| B、向久置于空气中的FeSO4溶液中滴加NaOH溶液,产生大量白色沉淀 |
| C、在空气中用酒精灯加热铝箔,铝箔熔化,失去光泽,但熔化的铝并不滴落 |
| D、向某溶液中滴加盐酸后,有能使澄清石灰水变浑浊的无色无味气体产生,证明该溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol NH3与1mol OH-所含的质子数均为10NA |
| B、常温下,pH=13的NaOH溶液中含OH-数目为NA |
| C、常温下,14g乙烯中含碳原子数为NA |
| D、标准状况下,22.4L CHCl3中含C-H键数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com