
在标准状况下,将1mol H2和11.2 L O2混合,得到气体的体积为( )
A.12.2 L B.<22.4 L C.33.6 L D.无法确定
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源:2017届北京市丰台区高三上学期期末化学试卷(解析版) 题型:选择题
室温下,向100 mL 0.1 mol/L NH4Cl溶液中加入下列物质。有关结论正确的是
加入的物质 | 结论 | |
A. | 100 mL 0.1 mol/L盐酸 | 溶液中2c(NH4+)= c(Cl-) |
B. | 0.01 mol Na2O2固体 | 反应完全后,溶液pH增大,c(Na+) = 2c(Cl-) |
C. | 100 mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
D. | 100 mL 0.1 mol/L NH3•H2O | 溶液中 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
Li-SOCl2电池是迄今具有最高能量比的电池。该电池中锂为负极,碳棒为正极,无水四氯铝酸锂(LiAlCl4)的SOCl2溶液为电解液。电池总反应为电池的总反应可表示为:4Li+2SOCl2= 4LiCl +SO2 +S。下列说法不正确的是
A.负极的电极反应式为 Li-e-=Li+
B.正极的电极反应式为2SOCl2+4e-=SO2+S+4Cl-
C.若电解液中含有水,则该电池的效率将大大降低
D.若负极有14gLi参加反应,则理论上流过电路中的电子书约为1.204×1023
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
已知A2On2-可与B2-反应,B2-被氧化,产物为B单质,A2On2-被还原,产物为A3+;且知100 mL c(A2On2-)= 0.3 mol/L的溶液与150 mL c(B2-)= 0.6 mol/L的溶液恰好完全反应,则n值为( )
A.4 B.5  C.7 D.6
C.7 D.6
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
下列叙述错误的是( )
A.酸、碱、盐、氧化物在组成上的共同点是都含有非金属元素
B.只含有一种元素的物质不一定都是纯净物
C.电离产生H+的化合物叫酸,其分子中氢原子的个数即是该酸的元数
D.压强恒定时,气体在水中的溶解度随温度的升高而降低
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
1 mol/L的硫酸溶液的含义是( )
mol/L的硫酸溶液的含义是( )
A.1L水中含有1molH2SO4 B.一定量的溶液中含有1molH2SO4
C.将98g浓硫酸溶于水配成1L溶液 D.指1L硫酸溶液中含 有98gH2SO4
有98gH2SO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:填空题
比较填空(填“>”、“<”或“=”)
(1)Ⅰ.比较等体积等浓度的溶液①盐酸 ②醋酸 与足量锌粒反应产生氢气的体积,① ②
Ⅱ.比较2H2(g)+O2(g) 2H2O(g) ΔH 1 2H2(g)+O2(g)
2H2O(g) ΔH 1 2H2(g)+O2(g) 2H2O(l) ΔH2的反应热 ΔH1 ΔH2
2H2O(l) ΔH2的反应热 ΔH1 ΔH2
Ⅲ.比较常温下两溶液水的电离程度,①pH=4盐酸 ②pH =10氨水溶液① ②
Ⅳ.同温度下溶液①使甲基橙呈现红色,溶液②使石蕊呈现紫色,比较两者pH① ②
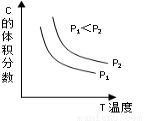
(2)Ⅴ.已知某可逆反应aA(g) + bB(g)  cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图,则a + b c + d
cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图,则a + b c + d
Ⅵ.比较①0.1mol/L醋酸与②0.01mol/L醋酸的导电能力,① ②
Ⅶ.1mol/L氨水与0.1mol/L氨水的c(OH-)之比 10
Ⅷ.体积相同的恒容密闭容器,在A中充入SO2和O2各1g,在B中充入SO2和O2各2g,相同条件下发生反应2SO2+O2 2SO3 平衡时 SO
2SO3 平衡时 SO 2的转化率A B
2的转化率A B
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
把一定浓度的NaOH溶液分成两等份,一份密闭保存,另一份敞口放置,几天后分别与相同浓度的盐酸反应,都恰好完全反应时,若第一份用去盐酸V1mL,第二份用去盐酸V2mL,则两者的关系为( )
A.V1=V2 B.V1>V2 C.V1<V2 D.不能确定
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上联考二化学卷(解析版) 题型:填空题
【化学—物质结构与性质】如右图是元素周期表的一部分。已知R的核电荷数小于36,气态氢化物沸点:MHn>YHn。
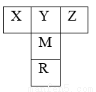
(1)表中五种元素第一电离能最大的是 (填元素符号),Y的最简单氢化物分子的空间构型为 ,基态R原子中有 个未成对电子。
(2)Y的最高价氧化物熔点比M的最高价氧化物熔点低,原因是 ,YZ-中σ键与π键的个数比为 。
(3)YO32-中Y原子的杂化方式是 ,写出一种与YO32-互 为等电子体的粒子 (用化学符号表示)。
为等电子体的粒子 (用化学符号表示)。
(4)Z的一种常见氢化物能与硫酸铜反应生成配合物。请用结构简式 表示该配合物中的阳离子: 。
表示该配合物中的阳离子: 。
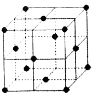
(5)如图为某金属单质的面心立方晶胞结构示意图,该晶体中配位数是 ;测得此晶体的密度为2.7g.cm-3,晶胞的边长为0.4 0
0 5nm,则此金属原子的相对原子质量为 (结果保留整数)。
5nm,则此金属原子的相对原子质量为 (结果保留整数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com