
【题目】电浮选凝聚法处理酸性污水的工作原理如图。下列说法正确的是
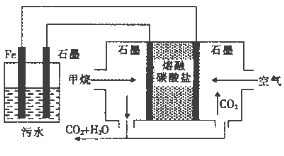
A. 左侧装置中的铁电极可换成石墨电极
B. 通入甲烷的石墨电极的电极反应式为: CH4+4CO32——8e—=5CO2+2H2O
C. 通入空气的石墨电极做正极,发生氧化反应
D. 若左侧装置中石墨电极产生标况下气体44.8L气体, 则消耗2mol甲烷
【答案】B
【解析】在甲烷燃料电池中,通入甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+ 4CO32--8e-=5CO2+2H2O,通入空气(氧气)的一极为原电池的正极,发生还原反应,电极方程式为O2+ 2CO2+4e-=2CO32-,铁连接原电池的正极,为电解池的阳极,被氧化,发生Fe-2e-=Fe2+,阴极生成2H++ 2e-=H2↑,A.铁连接原电池的正极,为电解池的阳极,被氧化,电极反应为Fe-2e-=Fe2+,因此左侧装置中的铁电极不能换成石墨电极,A错误; B.甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+4CO32--8e-=5CO2+2H2O,B正确;C. 通入空气的石墨电极做正极,发生还原反应,C错误;D. 左侧装置中石墨电极是阴极,氢离子放电,产生标况下气体44.8L气体, 即H2是2mol,转移4mol电子,根据电子转移守恒可知消耗甲烷4mol÷8=0.5mol,D错误;答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有Na+、Mg2+、Fe2+、H+、HCO3-、OH-、Cl-、NO3-、I-中的若干种,向该溶液中加入铝粉后,溶液中有AlO2-生成,则原溶液中能大最共存的离子最多有
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里保存下列试剂,其保存的方法和理由,描述都正确的是
编号 | 试剂 | 保存方法 | 理由 |
A | 水玻璃 | 存放在带橡皮塞的细口瓶中,密封 | 防止与空气接触被氧化和与二氧化碳接触而变质 |
B | 硫酸亚铁晶体 | 存放在带玻璃塞的广口瓶中,密封 | 防止与空气接触被氧化 |
C | 浓硫酸 | 密闭保存 | 防止吸水和挥发 |
D | 新制的溴水 | 存放在无色试剂瓶中,密封 | 防止挥发 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为CH2=CH— CH2OH。下列关于该有机物的叙述不正确的是
A.能与金属钠发生反应并放出氢气
B.能在催化剂作用下与H2发生加成反应
C.在浓H2SO4催化下能与乙酸发生酯化反应
D.能发生银境反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往含0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体的体积为6.72 L(标准状况下)时立即停止,则在这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【物质结构与性质】
氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1)与NF3分子互为等电子体的分子为 。
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式 。
写出该反应的化学方程式: 。

(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为____________mol。
(4)配合物丙的结构见图,丙中含有 (填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进入秋冬季节后,雾霾这种环境污染问题逐渐凸显。从物质分类来看雾霾属于胶体,它区别于溶液等其它分散系的本质特征是( )
A. 胶粒可以导电 B. 胶体具有丁达尔效应
C. 胶体粒子大小在1~100nm之间 D. 胶体的分散剂为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜基及硼系高温超导材料都具有良好的应用前景。回答下列问题:
(1)写出Cu原子价电子的轨道表达式:____________。BF3的立体构型是____________。
(2)NaBH4被认为是有机化学上的“万能还原剂”, NaBH4电子式为____________,其中三种元素的第一电离能由大到小的顺序是_________________。
(3)BH3·NH3是一种有效、安全的固体储氢材料,结构如右图所示。 B原子的轨道杂化类型是____________。该物质中含有配位键,其中提供空轨道接受孤对电子的是____________。该物质易溶于水,其原因是____________。
(4)硼与氦形成类似苯的化合物B3N3H6(硼氮苯),俗称无机苯。硼氮苯属于分子____________(填“极性”或“非极性”),一个硼氮苯分子中有____________个σ键,形成π键的电子由____________提供。
(5)硼与镁形成的高温超导材料晶体结构如图所示。该六方晶胞中镁原子与硼原子的数量比为____________,晶体密度d=____________g·cm-3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com