
| A. | 聚乙烯、淀粉 | B. | 油脂、蛋白质 | C. | 酚醛树脂、纤维素 | D. | 纤维素、淀粉 |
分析 高分子化合物(又称高聚物)一般相对分子质量高于10000,结构中有重复的结构单元;有机高分子化合物可以分为天然有机高分子化合物(如淀粉、纤维素、蛋白质天然橡胶等)和合成有机高分子化合物(如聚乙烯、聚氯乙烯等).
解答 解:A.淀粉是多糖,相对分子质量在一万以上,为天然高分子化合物,聚乙烯为合成高分子,故A错误;
B.蛋白质相对分子质量在一万以上,为天然高分子化合物,油脂相对分子质量不大,不是高分子化合物,故B错误;
C.酚醛树脂是利用缩聚反应生成的合成高分子化合物,为合成高分子化合物,故C错误;
D.淀粉、纤维素为多糖,相对分子质量在一万以上,为天然高分子化合物,故D正确.
故选D.
点评 本题考查合成材料等内容,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 18种 | C. | 21种 | D. | 36种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11H、21H、31H、H+和H2是氢元素的五种不同粒子 | |
| B. | 白磷和红磷的相互转化属于物理变化 | |
| C. | 11H和21H是不同的核素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
| A. | 单质的还原性:G<L<M | B. | 非金属性:T<Q | ||
| C. | 气态氢化物的稳定性:R>T | D. | L2+与T2-的核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻二溴苯只有一种可以证明苯环结构中不存在单双键交替结构 | |
| B. | 可以用分液漏斗分离苯和硝基苯 | |
| C. | 制取一氯乙烷的最佳途径是通过乙烷与氯气反应获得 | |
| D. | 等物质的量的乙醇和水分别与足量的钠反应,生成的气体体积比为3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 8种 | C. | 10种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
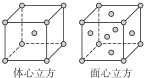
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

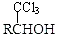 (-R表示烃基)
(-R表示烃基) .
. +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$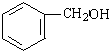 +NaCl.
+NaCl. +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.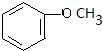 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com