
【题目】用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.1molO2与H2的混合气体中含有的分子数为NA
B.1.7g NH3所含原子数为0.1NA
C.通常状况下,11.2L N2中含有的原子数目为NA
D.标准状况下,22.4L H2O中含有的氧原子数为NA
科目:高中化学 来源: 题型:
【题目】按要求填空①写出硫酸铝的电离方程式 .
②写出稀硝酸跟氧化钠固体反应的离子方程式 .
③写出硫酸跟碳酸镁反应的离子方程式 .
④写出Cu2++2OH﹣═Cu(OH)2↓的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸是﹣种常见的有机酸,结构简式为 ![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.苹果酸能使紫色的石蕊试液变红
B.苹果酸能发生酯化反应
C.![]() 与苹果酸是同一种物质
与苹果酸是同一种物质
D.1mol苹果酸在一定条件下可与2molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A. 通常情况下,甲烷跟强酸、强碱和强氧化剂都不反应
B. 甲烷化学性质稳定,不能被任何氧化剂氧化
C. 甲烷与Cl2反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应
D. 甲烷的四种有机取代产物有一种气态,其余三种为液态且都不溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液显碱性,发生反应的离子方程式为 . ②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,写出发生反应的离子方程式 .
③对比①和②实验所得的结果,将I2、ClO﹣、SO ![]() 按氧化性由强到弱的顺序排列为 .
按氧化性由强到弱的顺序排列为 .
(2)今有铁皮、铜片、酸、碱、盐溶液若干.设计实验证明以下事实,写出反应的化学方程式.①浓硫酸的氧化性比稀硫酸强: .
②氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强: .
③铁的还原性比铜强: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵俗名摩尔盐.化学式为x(NH4)2SO4yFeSO4zH2O,可用来净水或治疗缺铁性贫血等.某实验小组利用下面的方法来测定其组成.
①NH4+含量测定:称取9.8g硫酸亚铁铵晶体,加适量水溶解,注人如图所示的三颈瓶中,然后逐滴加人足量lO%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用lOOmL 1.0molL﹣1的盐酸标准溶液吸收.
蒸氨结束后取下接收瓶,用1.0molL﹣1NaOH标准溶液滴定剩余的HCl,到终点时消耗50mlNaOH溶液.
②Fe2+含量测定:向上述实验后的三颈瓶中加入过量的3%的双氧水,充分反应后过滤、洗涤、灼烧得到2.0g固体.
③结晶水含量测定:称取9.8g硫酸亚铁铵晶体,在质量为15g的坩埚中加热至200℃,恒温一段时间,置于空气中冷却,称量质量为22.3g;重复上述加热、冷却、称量过程,发现两次称量结果相同.回答下列问题: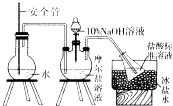
(1)装置中安全管的作用原理是 .
(2)冰盐水的作用是 .
(3)用NaOH标准溶液滴定剩余的HCl时,可使用的指示剂是 .
(4)测定Fe2+时.加人双氧水发生反应的化学方程式是 .
(5)如果在测定NH4+含量的过程中,亚铁元素部分被氧化,对Fe2+含量的测定(填“有”或“无”)影响.
(6)根据①、②的数据,该摩尔盐晶体中n(NH4+):n(Fe2+):n(SO42﹣ )= , z= .
(7)根据③的数据,发现结晶水含量测定结果偏低.从实验过程分析,可能原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属单质及其化合物常应用于有机物的反应和分析之中,某芳香族化合物A分子式为C8H10O2 , 为测定其结构做如下分析:
(1)为确定羟基的个数,将1mol A与足量钠反应生成氢气22.4L(标准状况下),说明A分子中含羟基个.
(2)核磁共振氢谱显示A有3个峰,峰面积之比为1:2:2,该物质的结构简式为 .
(3)A在Cu催化下可被氧气氧化生成有机物B,B的相对分子质量比A小4.试写出反应的方程式 .
(4)1mol B与足量银氨溶液充分反应生成有机物C,同时得到银克.试写出化学反应方程式 . (原子量:Ag﹣﹣108)
(5)有机物F是有机物B的一种同分异构体.1mol F与足量钠反应同样生成氢气22.4L(标准状况下),且F能使氯化铁溶液显紫色.试写出满足此条件的有机物F的结构简式(只写出一种即可).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com